مقدمه
مغز انسان سالم حاوی ده ها میلیارد نورون است. سلول های تخصصی که اطلاعات را از طریق سیگنال های الکتریکی و شیمیایی پردازش و منتقل می کنند. آنها پیام هایی را بین قسمت های مختلف مغز و از مغز به عضلات و اندام های بدن ارسال می کنند. بیماری آلزایمر این ارتباط بین نورون ها را مختل می کند. درنتیجه منجر به از دست دادن عملکرد و مرگ سلولی می شود.
فرآیندهای بیولوژیکی کلیدی در مغز
اکثر نورون ها دارای سه بخش اصلی هستند: جسم سلولی، دندریت های متعدد و آکسون. جسم سلولی حاوی هسته است که طرح ژنتیکی را در خود جای داده است که فعالیت های سلول را هدایت و تنظیم می کند. دندریت ها ساختارهای شاخه مانندی هستند که از بدن سلولی گسترش یافته و اطلاعات را از سایر نورون ها جمع آوری می کنند. آکسون یک ساختار کابل مانند در انتهای بدنه سلولی در مقابل دندریت ها است و پیام ها را به نورون های دیگر منتقل می کند.
عملکرد و بقای نورون ها به چندین فرآیند بیولوژیکی کلیدی بستگی دارد:
ارتباط
نورون ها دائماً با سلول های مغزی مجاور در تماس هستند. هنگامی که یک نورون سیگنالهایی را از سایر نورونها دریافت میکند، بار الکتریکی تولید میکند. بار در طول آکسون خود حرکت میکند و مواد شیمیایی انتقالدهنده عصبی را در یک شکاف کوچک به نام سیناپس آزاد میکند. مانند کلیدی که در یک قفل قرار می گیرد. هر مولکول انتقال دهنده عصبی سپس به مکان های گیرنده خاصی در دندریت یک نورون مجاور متصل می شود. این فرآیند سیگنال های شیمیایی یا الکتریکی را تحریک می کند. باعث تحریک یا مهار فعالیت نورون دریافت کننده سیگنال می شود. ارتباط اغلب در میان شبکه های سلول های مغز رخ می دهد. در واقع، دانشمندان تخمین می زنند که در شبکه ارتباطی مغز، یک نورون ممکن است 7000 ارتباط سیناپسی با نورون های دیگر داشته باشد.
متابولیسم
متابولیسم یعنی تجزیه مواد شیمیایی و مواد مغذی در یک سلول که برای عملکرد و بقای سلول سالم حیاتی است. برای انجام این عملکرد، سلول ها به انرژی به شکل اکسیژن و گلوکز نیاز دارند. که از طریق گردش خون در مغز تامین می شود. مغز یکی از غنی ترین ذخایر خون را در بین هر اندامی دارد. تا 20 درصد انرژی مصرف شده توسط بدن انسان را مصرف می کند – بیش از هر اندام دیگری.
ترمیم
برخلاف بسیاری از سلولهای بدن که عمر نسبتاً کوتاهی دارند، نورونها برای مدت طولانی – بیش از 100 سال در انسان – تکامل یافتهاند. در نتیجه، نورون ها باید دائماً خود را حفظ و ترمیم کنند. نورونها همچنین به طور پیوسته اتصالات سیناپسی خود را بسته به میزان تحریکی که از سایر نورونها دریافت میکنند، تنظیم یا «بازسازی» میکنند. به عنوان مثال، آنها ممکن است اتصالات سیناپسی را تقویت یا تضعیف کنند. یا حتی ارتباط با یک گروه از نورون ها را از بین ببرند و ارتباطات جدیدی با گروه دیگری ایجاد کنند. مغز بزرگسالان حتی ممکن است نورون های جدیدی تولید کند. فرآیندی که نوروژنز نام دارد. بازسازی اتصالات سیناپسی و نوروژنز برای یادگیری، حافظه و احتمالاً ترمیم مغز مهم است.
نورون ها بازیگر اصلی سیستم عصبی مرکزی هستند، اما انواع سلول های دیگر نیز کلید عملکرد سالم مغز هستند.
در واقع، سلولهای گلیال بسیار پرتعدادترین سلولها در مغز هستند و تعداد آنها از نورونها حدود 10 تا 1 بیشتر است. این سلولها که به اشکال مختلف مانند میکروگلیا، آستروسیت و الیگودندروسیت وجود دارند. عملکرد و سلامتی را احاطه کرده و از آن پشتیبانی میکنند. به عنوان مثال، میکروگلیا از نورون ها در برابر آسیب فیزیکی و شیمیایی محافظت می کند و مسئول پاکسازی مواد خارجی و باقی مانده های سلولی از مغز است. برای انجام این عملکردها، سلول های گلیال اغلب با رگ های خونی در مغز همکاری می کنند. سلولهای گلیال و رگهای خونی با هم تعادل ظریف مغز را تنظیم میکنند. تا اطمینان حاصل شود که بهترین عملکرد را دارد.
چگونه بیماری آلزایمر بر مغز تأثیر می گذارد؟
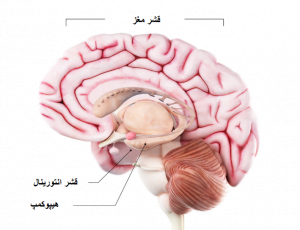
مغز معمولاً در پیری سالم تا حدودی کوچک میشود. اما در کمال تعجب، سلولهای عصبی را به تعداد زیاد از دست نمیدهد. با این حال، در بیماری آلزایمر، آسیب گسترده است. زیرا بسیاری از نورونها کار نمیکنند. ارتباط خود را با سایر نورونها از دست میدهند و میمیرند. آلزایمر فرآیندهای حیاتی برای نورون ها و شبکه های آنها از جمله ارتباطات، متابولیسم و ترمیم را مختل می کند. در ابتدا، بیماری آلزایمر به طور معمول نورون ها و اتصالات آنها را در بخش هایی از مغز که درگیر حافظه هستند، از جمله قشر انتورینال و هیپوکامپ را از بین می برد. بعداً بر نواحی در قشر مغز که مسئول زبان، استدلال و رفتار اجتماعی هستند تأثیر می گذارد. در نهایت، بسیاری از نواحی دیگر مغز آسیب می بینند.
با گذشت زمان، فرد مبتلا به آلزایمر به تدریج توانایی زندگی و عملکرد مستقل خود را از دست می دهد. در نهایت این بیماری کشنده است.
ویژگی های اصلی مغز مبتلا به آلزایمر چیست؟
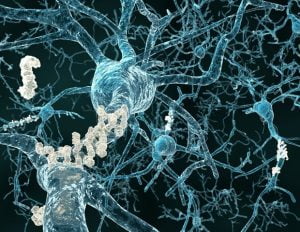
بسیاری از تغییرات مولکولی و سلولی در مغز افراد مبتلا به آلزایمر رخ می دهد. این تغییرات را می توان پس از مرگ در بافت مغز زیر میکروسکوپ مشاهده کرد. تحقیقات برای تعیین اینکه کدام تغییرات ممکن است باعث آلزایمر شود و کدام یک نتیجه این بیماری باشد در حال انجام است.
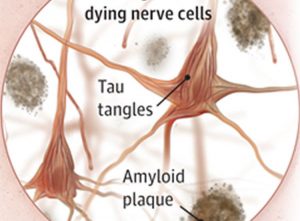
پلاک های آمیلوئید
پروتئین بتا آمیلوئید دخیل در آلزایمر در چندین شکل مولکولی مختلف وجود دارد که بین نورون ها جمع می شود. این پروتئین از تجزیه یک پروتئین بزرگتر به نام پروتئین پیش ساز آمیلوئید تشکیل می شود. تصور می شود که یکی از آن ها، بتا آمیلوئید 42، سمی است. در مغز آلزایمری، سطوح غیرطبیعی این پروتئین طبیعی به هم می پیوندند و پلاک هایی را تشکیل می دهند. پلاک ها بین نورون ها جمع می شوند و عملکرد سلول را مختل می کنند. تحقیقات برای درک بهتر نحوه و در چه مرحله ای از بیماری، اشکال مختلف بتا آمیلوئید بر آلزایمر تأثیر می گذارد، ادامه دارد.
گره های نوروفیبریلاری
تجمع غیرطبیعی پروتئینی به نام تائو هستند که درون نورونها جمع میشوند. نورون های سالم تا حدی توسط ساختارهایی به نام میکروتوبول ها پشتیبانی می شوند. که به هدایت مواد مغذی و مولکول ها از بدن سلولی به آکسون و دندریت کمک می کنند. در نورون های سالم، تائو به طور معمول به میکروتوبول ها متصل می شود و آنها را تثبیت می کند. با این حال، در بیماری آلزایمر، تغییرات شیمیایی غیرعادی باعث جدا شدن تائو از میکروتوبولها و چسبیدن به مولکولهای دیگر تائو میشود. رشتههایی را تشکیل میدهند که در نهایت به هم میپیوندند و درون نورونها به هم گره میخورند. این گرهها سیستم انتقال نورون را مسدود میکنند که به ارتباط سیناپسی بین نورونها آسیب میزند.
شواهد در حال ظهور نشان می دهد:
تغییرات مغزی مرتبط با آلزایمر ممکن است ناشی از یک تعامل پیچیده بین پروتئین های غیر طبیعی تائو و بتا آمیلوئید و چندین عامل دیگر باشد. به نظر می رسد که تائو غیرطبیعی در مناطق خاصی از مغز که درگیر حافظه هستند تجمع می یابد. بتا آمیلوئید به پلاک های بین نورون ها تبدیل می شود. با رسیدن سطح بتا آمیلوئید به نقطه اوج، انتشار سریع تائو در سراسر مغز وجود دارد.
التهاب مزمن
تحقیقات نشان می دهد که التهاب مزمن ممکن است ناشی از تجمع سلول های گلیال باشد. سلول هایی که به طور معمول به مغز کمک می کنند تا از خطر ذرات باقی مانده در امان باشد. یکی از انواع سلول های گلیال، میکروگلیا، مواد زائد و سموم را در مغز سالم می بلعد و از بین می برد. در آلزایمر، میکروگلیا نمیتواند زبالهها و مجموعههای پروتئینی از جمله پلاکهای بتا آمیلوئید را پاک کند. محققان در تلاشند تا دریابند چرا میکروگلیا در انجام این عملکرد حیاتی در آلزایمر ناتوان است.
یکی از محورهای مطالعه، ژنی به نام TREM2 است.
به طور معمول، TREM2 به سلول های میکروگلیا می گوید که پلاک های بتا آمیلوئید را از مغز پاک کنند و به مبارزه با التهاب در مغز کمک می کند. در مغز افرادی که این ژن به طور طبیعی عمل نمی کند، پلاک هایی بین نورون ها ایجاد می شود. آستروسیتها – نوع دیگری از سلولهای گلیال – برای کمک به پاکسازی تجمع پلاکها و سایر بقایای سلولی به جا مانده اند. این میکروگلیاها و آستروسیتها در اطراف نورونها جمع میشوند. اما در انجام عملکرد پاکسازی زبالهها ناکام هستند. علاوه بر این، آنها مواد شیمیایی آزاد می کنند که باعث التهاب مزمن می شود. به نورون هایی که قرار است از آنها محافظت کنند آسیب بیشتری می رساند.
مشارکت عروقی در بیماری آلزایمر
افراد مبتلا به زوال عقل به ندرت فقط تغییرات مرتبط با آلزایمر در مغز خود دارند. هر تعدادی از مشکلات عروقی – مشکلاتی که رگهای خونی را تحت تأثیر قرار میدهند، مانند رسوبات بتا آمیلوئید در شریانهای مغز، آترواسکلروز (سخت شدن شریانها) و سکتههای کوچک نیز ممکن است مطرح شوند. مشکلات عروقی ممکن است منجر به کاهش جریان خون و اکسیژن به مغز شوند.همچنین موجب شکسته شدن سد خونی مغزی شده که معمولاً مغز را در برابر عوامل مضر محافظت می کند. و در عین حال اجازه ورود گلوکز و سایر عوامل ضروری را می دهد. در یک فرد مبتلا به آلزایمر، یک سد خونی مغزی معیوب از رسیدن گلوکز به مغز جلوگیری می کند. همچنین از پاک شدن پروتئین های سمی بتا آمیلوئید و تائو جلوگیری می کند.
در نهایت
این مشکلات هم منجر به التهاب می شود که خود به مشکلات عروقی در مغز می افزاید. از آنجا که به نظر می رسد آلزایمر هم علت و هم پیامد مشکلات عروقی در مغز است، محققان به دنبال مداخلاتی هستند تا این چرخه پیچیده و مخرب را مختل کنند.
از دست دادن اتصالات عصبی و مرگ سلولی در بیماری آلزایمر
زمانی که نورونها در سراسر مغز آسیب میبینند و میمیرند، اتصالات بین شبکههای عصبی ممکن است از بین برود. درنتیجه بسیاری از مناطق مغز شروع به کوچک شدن می کنند. در مراحل پایانی آلزایمر، این فرآیند – که آتروفی مغز نامیده می شود – گسترده است. باعث کاهش قابل توجه حجم مغز می شود.
منبع: What Happens to the Brain in Alzheimer’s Disease? | National Institute on Aging (nih.gov)

درباره نویسنده
خجسته رحیمی جابری، پژوهشگر دکترای تخصصی علوم اعصاب دانشگاه علوم پزشکی شیراز و نویسنده وب سایت انستیتو سلامت مغز دانا. زمینه کاری تخصصی ایشان مشکلات حافظه و آلزایمر است وی بیش از 20 مقاله معتبر بین المللی در این زمینه به چاپ رسانده است. می توانید پژوهش های او را در اینجا (کلیک کنید) دنبال کنید.