میاستنی گراویس
میاستنی گراویس یک بیماری مزمن خود ایمنی و عصبی-عضلانی است. باعث ضعف در عضلات اسکلتی می شود. این ضعف عضلانی، پس از دوره های فعالیت بدتر می شود و پس از دوره های استراحت بهبود می یابد. ماهیچه ها، وظیفه تنفس و حرکت در قسمت های بدن از جمله بازوها و پاها را بر عهده دارند.
میاستنی گراویس، در اصل به معنای “ضعف شدید یا جدی عضلانی” است. برای این بیماری، هیچ درمان شناخته شده ای وجود ندارد. درمان های موجود می توانند علائم را کنترل کرده و اغلب به افراد اجازه می دهند کیفیت زندگی نسبتاً بالایی داشته باشند. بیشتر افراد مبتلا به این بیماری، امید به زندگی طبیعی دارند.
علائم میاستنی گراویس چیست؟
ویژگی بارز میاستنی گراویس، ضعف عضلانی است که پس از دوره های فعالیت بدتر می شود و پس از دوره های استراحت بهبود می یابد. ماهیچه های خاصی مانند ماهیچه های کنترل کننده حرکت چشم و پلک، حالت دهنده صورت، جویدن، صحبت کردن و بلعیدن، اغلب (اما نه همیشه) در این اختلال دخیل هستند.
شروع این اختلال ممکن است ناگهانی باشد. علائم، اغلب بلافاصله به عنوان میاستنی گراویس شناخته نمی شوند. میزان ضعف عضلانی مربوط به میاستنی گراویس در افراد مختلف بسیار متفاوت است.
افراد مبتلا به میاستنی گراویس ممکن است علائم زیر را تجربه کنند:
- ضعف عضلات چشم (میاستنی چشمی نامیده می شود)
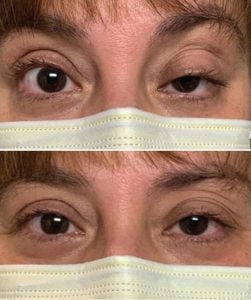
- افتادگی یک یا هر دو پلک (پتوز)
- تاری دید یا دوبینی (دوبینی)
- تغییر حالت چهره
- مشکل بلع
- تنگی نفس
- اختلال در گفتار (دیسارتری)
- ضعف در بازوها، دستها، انگشتان، پاها و گردن.
بحران میاستنی چیست؟
بحران میاستنی، یک فوریت پزشکی است و زمانی رخ می دهد که ماهیچه های کنترل کننده تنفس، ضعیف می شوند. تا جایی که افراد برای تنفس به یک دستگاه تنفس نیاز دارند. بحران بیماری ممکن است در اثر عفونت، استرس، جراحی یا واکنش نامطلوب به دارو ایجاد شود.
تقریباً 15 تا 20 درصد از افراد مبتلا به میاستنی گراویس، حداقل یک بحران میاستنی را تجربه می کنند. با این حال، تا نیمی از افراد ممکن است هیچ دلیل واضحی برای بحران میاستنی خود نداشته باشند.
برخی از داروها باعث ایجاد علائم میاستنی گراویس می شوند. با این حال، گاهی اوقات در صورت اهمیت بیشتر برای درمان بیماری زمینه ای، ممکن است از این داروها استفاده شود.
علت میاستنی گراویس چیست؟
آنتی بادی ها
میاستنی گراویس یک بیماری خود ایمنی است. به این معنی که سیستم ایمنی بدن – که به طور معمول بدن را در برابر موجودات خارجی محافظت می کند – به اشتباه به خود حمله می کند.
بیماری در اثر خطای انتقال تکانه های عصبی به ماهیچه ها ایجاد می شود. این اتفاق زمانی رخ می دهد که ارتباط عادی بین عصب و عضله در محل اتصال عصبی –عضلانی، جایی که سلول های عصبی با ماهیچه های تحت کنترل خود متصل می شوند، قطع می شود.
انتقال دهنده های عصبی، مواد شیمیایی هستند که نورون ها یا سلول های مغزی از آنها برای انتقال اطلاعات استفاده می کنند. به طور معمول هنگامی که سیگنال های الکتریکی یا تکانه ها به سمت یک عصب حرکتی حرکت می کنند، پایانه عصبی، یک انتقال دهنده عصبی به نام استیل کولین، آزاد می کند.
استیل کولین، به مکان هایی به نام گیرنده های استیل کولین روی عضله متصل می شود. اتصال استیل کولین به گیرنده آن، باعث فعال شدن ماهیچه و انقباض ماهیچه می شود.
در میاستنی گراویس، آنتی بادی ها (پروتئین های تولید شده توسط سیستم ایمنی بدن)، گیرنده های استیل کولین را در محل اتصال عصبی-عضلانی مسدود می کنند. ممکن است آنها را تغییر داده یا از بین ببرد.
درنتیجه از انقباض ماهیچه جلوگیری می کند. این اتفاق اغلب در اثر آنتی بادی های گیرنده استیل کولین ایجاد می شود. اما آنتی بادی های دیگر مانند پروتئین MuSK (کیناز مخصوص عضلات) نیز می توانند انتقال را در محل اتصال عصبی- عضلانی مختل کنند.
غده تیموس
غده تیموس عملکرد سیستم ایمنی را کنترل می کند. ممکن است با میاستنی گراویس در ارتباط باشد. تیموس تا بلوغ به تدریج رشد می کند و سپس کوچکتر می شود و چربی جایگزین آن می شود.
در طول دوران کودکی، تیموس نقش مهمی در توسعه سیستم ایمنی بدن ایفا می کند. زیرا مسئول تولید لنفوسیت های T یا سلول هایT، است. نوعی خاص از گلبول های سفید خون که بدن را در برابر ویروس ها و عفونت ها محافظت می کند.
در بسیاری از بزرگسالان مبتلا به میاستنی گراویس، غده تیموس بزرگ باقی می ماند. افراد مبتلا به این بیماری معمولاً دارای خوشه ای از سلول های ایمنی در غده تیموس خود هستند. ممکن است به تیموما (تومورهای غده تیموس) مبتلا شوند.
تیموما اغلب بی ضرر هستند اما می توانند سرطانی شوند. دانشمندان معتقدند غده تیموس ممکن است دستورالعمل های نادرستی به سلول های ایمنی بدن بدهد. در نهایت باعث شود که سیستم ایمنی بدن به سلول ها و بافت های خود حمله کرده و آنتی بادی های گیرنده استیل کولین را تولید کند. همین امر زمینه را برای حمله به اتصال عصبی-عضلانی فراهم می کند.
چه کسی به میاستنی گراویس مبتلا می شود؟
میاستنی گراویس هم بر مردان و هم زنان تأثیر می گذارد و در همه گروه های نژادی و قومی رخ می دهد. این بیماری، بیشتر زنان جوان (زیر 40 سال) و مردان مسن (بالای 60 سال) را تحت تاثیر قرار می دهد. اما می تواند در هر سنی، از جمله دوران کودکی رخ دهد.
میاستنی گراویس موروثی یا مسری نیز نیست. گاهی اوقات، این بیماری ممکن است در بیش از یک عضو از یک خانواده رخ دهد. اگرچه میاستنی گراویس به ندرت در نوزادان دیده می شود، اما جنین ممکن است آنتی بادی هایی را از مادری که مبتلا به میاستنی گراویس است، بدست آورد. به این حالت، میاستنی نوزادی گفته می شود.
میاستنی گراویس نوزادان
به طور کلی موقتی است و علائم کودک معمولاً ظرف دو تا سه ماه پس از تولد از بین می روند. به ندرت، فرزندان یک مادر سالم ممکن است دچار میاستنی مادرزادی شوند. این یک اختلال خود ایمنی نیست بلکه ناشی از ژن های معیوب است که پروتئین های غیر طبیعی را در محل اتصال عصبی -عضلانی تولید می کنند. می توانند علائم مشابهی را در میاستنی گراویس ایجاد کنند.
میاستنی گراویس چگونه تشخیص داده می شود؟
پزشک ممکن است آزمایش های متعددی را برای تأیید تشخیص میاستنی گراویس انجام دهد. ابتدا سابقه پزشکی افراد را بررسی کرده و معاینه فیزیکی انجام می دهد. در معاینه عصبی، پزشک قدرت و تون عضلات، هماهنگی و حس لامسه را بررسی می کند. همچنین نقص حرکات چشم را نیز بررسی می کند.
آزمایش ادروفونیم
در این آزمایش از تزریق کلرید ادروفونیوم برای رفع کوتاه مدت ضعف در افراد مبتلا به میاستنی گراویس استفاده می شود. این دارو تجزیه استیل کولین را مسدود کرده و به طور موقت سطوح استیل کولین را در محل اتصال عصبی عضلانی افزایش می دهد. معمولاً برای آزمایش ضعف عضلات چشم استفاده می شود.
آزمایش خون
بیشتر افراد مبتلا به میاستنی گراویس دارای سطوح غیرطبیعی آنتی بادی های گیرنده استیل کولین هستند. آنتی بادی دوم-به نام آنتی بادی anti-MuSK-در حدود نیمی از افراد مبتلا به میاستنی گراویس که آنتی بادی گیرنده استیل کولین ندارند، یافت شده است.
از طریق آزمایش خون نیز می توان این آنتی بادی را تشخیص داد. با این حال، در برخی از افراد مبتلا به میاستنی گراویس، هیچ یک از این آنتی بادی ها وجود ندارد. گفته می شود این افراد میاستنی سرونگاتیو (آنتی بادی منفی) دارند.
تشخیص همچنین با تحریک مکرر عصب نیز انجام می شود.
روشی که به طور مکرر، اعصاب فرد را با پالس های الکتریکی کوچک تحریک می کند تا ماهیچه های خاص را خسته کند. فیبرهای عضلانی در میاستنی گراویس و سایر اختلالات عصبی -عضلانی در مقایسه با ماهیچه های افراد عادی، به تحریک الکتریکی مکرر پاسخ نمی دهند.
الکترومیوگرافی تک فیبر (EMG)، که حساس ترین آزمایش برای میاستنی گراویس محسوب می شود، اختلال در انتقال عصب به عضله را تشخیص می دهد. این روش، در تشخیص موارد خفیف میاستنی گراویس در مواردی که سایر آزمایشات، ناهنجاری ها را نشان نمی دهند، بسیار مفید است.
تصویربرداری
تصویربرداری تشخیصی از قفسه سینه با استفاده از توموگرافی کامپیوتری (CT) یا تصویربرداری رزونانس مغناطیسی (MRI) ممکن است وجود تیموما را مشخص کند.
اندازه گیری قدرت تنفس
می تواند به پیش بینی اینکه آیا تنفس ممکن است شکست بخورد و منجر به بحران میاستنی شود، کمک کند. از آنجا که ضعف، یک علامت شایع در بسیاری از اختلالات دیگر است، تشخیص میاستنی گراویس، اغلب در افرادی که ضعف خفیفی دارند یا در افرادی که ضعف آنها محدود به چند عضله است، گاهی تا دو سال با تاخیر انجام می شود.
میاستنی گراویس چگونه درمان می شود؟
امروزه میاستنی گراویس به طور کلی قابل کنترل است. چندین روش درمانی موجود برای کاهش و بهبود ضعف عضلانی وجود دارد.
برداشتن غده تیموس (که اغلب در افراد مبتلا به میاستنی گراویس به صورت غیرطبیعی است) می تواند علائم را کاهش داده و برخی افراد را احتمالاً با ایجاد تعادل مجدد در سیستم ایمنی درمان کند.
تیمکتومی هم برای افراد مبتلا به تیموما و هم برای افرادی که هیچ شواهدی از تومورها ندارند مفید است. این جراحی، ضعف عضلانی و نیاز به داروهای سرکوب کننده سیستم ایمنی را کاهش می دهد.
آنتی بادی مونوکلونال
این درمان فرآیندی را هدف می گیرد که طی آن آنتی بادی های استیل کولین به اتصال عصبی عضلانی آسیب می رسانند. در سال 2017، سازمان غذا و داروی ایالات متحده استفاده از eculizumab را برای درمان میاستنی گراویس عمومی در بزرگسالانی که تست آنتی بادی گیرنده آنتی استیل کولین (AchR) مثبت بود، تایید کرد.
داروهای درمان این اختلال، شامل داروهای آنتی کولین استراز مانند پیریدوستیگمین است که تجزیه استیل کولین را در محل اتصال عصبی- عضلانی کند می کند. در نتیجه انتقال عصبی -عضلانی را بهبود می بخشد و قدرت عضلات را افزایش می دهد.
داروهای سرکوب کننده سیستم ایمنی با سرکوب تولید آنتی بادی های غیرطبیعی، قدرت ماهیچه ها را افزایش می دهند. آنها شامل پردنیزولون، آزاتیوپرین، مایکوفنولات موفتیل و تاکرولیموس هستند. این داروها می توانند عوارض جانبی قابل توجهی را ایجاد کنند و باید به دقت توسط پزشک نظارت شود.
پلاسمافرز و ایمونوگلوبولین داخل وریدی، ممکن است در موارد شدید میاستنی گراویس گزینه های کمک کننده باشند. افراد می توانند آنتی بادی هایی در پلاسمای خود (جزء مایع در خون) داشته باشند که به محل اتصال عصبی-عضلانی حمله می کنند. این درمان ها آنتی بادی های مخرب را حذف می کند، اگرچه اثربخشی آنها معمولاً فقط چند هفته تا چند ماه طول می کشد.
پلاسمافرزیس روشی است که از دستگاه برای حذف آنتی بادی های مضر در پلاسما و جایگزینی آنها با پلاسما خوب یا جایگزین پلاسما استفاده می شود.
ایمونوگلوبولین داخل وریدی یک تزریق بسیار غلیظ آنتی بادی است که از بسیاری از اهداکنندگان سالم جمع شده است و به طور موقت نحوه عملکرد سیستم ایمنی را تغییر می دهد. این ماده با اتصال به آنتی بادی های ایجاد کننده میاستنی گراویس و حذف آنها از گردش خون عمل می کند.
پیش آگهی چیست؟
با درمان، اکثر افراد مبتلا به میاستنی می توانند ضعف عضلانی خود را به میزان قابل توجهی بهبود بخشند و زندگی عادی یا تقریباً عادی را تجربه کنند.
برخی از موارد میاستنی گراویس ممکن است به طور موقت یا دائمی بهبود پیدا کنند. ضعف عضلانی ممکن است به طور کامل از بین برود تا مصرف دارو قطع شود. بهبودی کامل پایدار و طولانی مدت، هدف از عمل جراحی است و ممکن است در 50 درصد افرادی که تحت این روش قرار می گیرند رخ دهد.
گزینه های درمانی جدید
یافته های یک مطالعه اخیر با پشتیبانی NINDS شواهد قطعی در مورد مزایای عمل جراحی برای افراد بدون تیموما را فراهم کرد، موضوعی که دهه ها مورد بحث قرار گرفته بود. محققان امیدوارند این آزمایش به الگویی برای آزمایش دقیق سایر گزینه های درمانی تبدیل شود و سایر مطالعات به بررسی درمان های مختلف ادامه دهند تا ببینند آیا آنها بر گزینه های استاندارد مراقبت برتری دارند یا خیر.
فناوری های کمکی مانند دستگاه های مغناطیسی نیز ممکن است به افراد مبتلا به میاستنی گراویس در کنترل برخی از علائم این اختلال کمک کند.
خجسته رحیمی جابری
پژوهشگر دکتری تخصصی علوم اعصاب
برای اطلاعات بیشتر درباره راهکارهای درمانی جدید در میاستنی گراویس، با ما در انستیتو سلامت مغز دانا در تماس باشید.

درباره نویسنده
خجسته رحیمی جابری، پژوهشگر دکترای تخصصی علوم اعصاب دانشگاه علوم پزشکی شیراز و نویسنده وب سایت انستیتو سلامت مغز دانا. زمینه کاری تخصصی ایشان مشکلات حافظه و آلزایمر است وی بیش از 20 مقاله معتبر بین المللی در این زمینه به چاپ رسانده است. می توانید پژوهش های او را در اینجا (کلیک کنید) دنبال کنید.