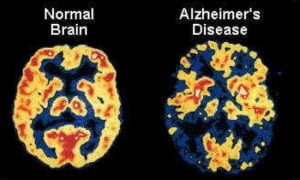
علائم بیماری آلزایمر چیست؟
دانشمندان به کشف تغییرات پیچیده مغزی که در شروع و پیشرفت بیماری آلزایمر نقش دارند، ادامه می دهند. به نظر می رسد که آسیب به مغز یک دهه یا بیشتر قبل از ظهور حافظه و سایر مشکلات شناختی شروع می شود. در طول این مرحله پیش بالینی بیماری آلزایمر، به نظر می رسد افراد بدون علامت هستند. اما تغییرات سمی در مغز در حال وقوع است. آسیبی که در مغز فرد مبتلا به بیماری آلزایمر رخ می دهد، در علائم و نشانه های بالینی بسیار اولیه خود را نشان می دهد. برای اکثر افراد مبتلا به آلزایمر – کسانی که نوع دیررس آن را دارند – علائم برای اولین بار در اواسط دهه 60 زندگی ظاهر می شوند. علائم آلزایمر زودرس بین 30 تا 60 سالگی شروع می شود.
اولین علائم آلزایمر از فردی به فرد دیگر متفاوت است.
مشکلات حافظه معمولاً یکی از اولین نشانه های اختلال شناختی مرتبط با بیماری آلزایمر است. کاهش در جنبههای غیرحافظه شناختی، مانند واژهیابی، مسائل بینایی/فضایی، و اختلال در استدلال یا قضاوت نیز ممکن است نشانهای از مراحل اولیه بیماری آلزایمر باشد. برخی افراد ممکن است با اختلال شناختی خفیف تشخیص داده شوند. با پیشرفت بیماری، افراد از دست دادن حافظه و سایر مشکلات شناختی بیشتری را تجربه می کنند. بیماری آلزایمر در چند مرحله پیشرفت میکند. پیش بالینی، خفیف (گاهی اوقات مرحله اولیه نامیده میشود)، متوسط و شدید (گاهی اوقات مرحله آخر نامیده میشود).
علائم نوع خفیف بیماری آلزایمر
در بیماری آلزایمر خفیف، ممکن است فرد سالم به نظر برسد. اما در درک دنیای اطرافش مشکل بیشتری دارد. درک اینکه چیزی اشتباه است اغلب به تدریج به خود شخص و خانواده اش می رسد. مشکلات می تواند شامل موارد زیر باشد:
- از دست دادن حافظه.
- قضاوت ضعیف که منجر به تصمیمات بد می شود.
- از دست دادن انگیزه و ابتکار عمل.
- زمان بیشتری برای انجام کارهای عادی روزانه نیاز دارد.
- سوالات تکراری
- مشکل در رسیدگی به پول و پرداخت قبوض.
- سرگردانی و گم شدن.
- فراموش کردن وسایل یا قرار دادن آنها در مکان های عجیب و غریب.
- خلق و خو و شخصیت تغییر می کند.
- افزایش اضطراب و/یا پرخاشگری.
- بیماری آلزایمر اغلب در این مرحله تشخیص داده می شود.
علائم نوع متوسط بیماری آلزایمر
در این مرحله نظارت و مراقبت شدیدتر ضروری می شود که برای بسیاری از همسران و خانواده ها دشوار است. علائم ممکن است شامل موارد زیر باشد:
- افزایش از دست دادن حافظه و سردرگمی
- ناتوانی در یادگیری چیزهای جدید
- مشکل در زبان و مشکل در خواندن، نوشتن و کار با اعداد
- مشکل در سازماندهی افکار و تفکر منطقی
- کوتاه شدن دامنه توجه
- مشکلات کنار آمدن با موقعیت های جدید
- مشکل در انجام وظایف چند مرحله ای، مانند پوشیدن لباس
- مشکلات در شناخت خانواده و دوستان
- توهم، هذیان و پارانویا
- رفتارهای تکانشی مانند درآوردن لباس در زمان ها یا مکان های نامناسب یا استفاده از الفاظ رکیک
- طغیان های نامناسب
- عصبانیت
- بی قراری، اضطراب، اشک ریختن
- سرگردانی – به خصوص در اواخر بعد از ظهر یا عصر
- جملات یا حرکت های تکراری، گهگاهی انقباضات عضلانی
علائم نوع شدید بیماری آلزایمر
افراد مبتلا به آلزایمر شدید نمی توانند ارتباط برقرار کنند. برای مراقبت از خود کاملاً به دیگران وابسته هستند. در مراحل پایانی، ممکن است فرد بیشتر یا تمام اوقات در رختخواب باشد. زیرا بدن از کار می افتد. علائم آنها اغلب عبارتند از:
- ناتوانی در برقراری ارتباط
- کاهش وزن
- تشنج
- عفونت های پوستی
- مشکل در بلع
- ناله یا غرغر کردن
- افزایش خواب
- از دست دادن کنترل روده و مثانه
- یکی از علل شایع مرگ افراد مبتلا به آلزایمر، پنومونی آسپیراسیون است. این نوع ذات الریه زمانی ایجاد می شود که فرد نتواند به درستی قورت دهد و غذا یا مایعات را به جای هوا وارد ریه کند.
- در حال حاضر هیچ درمانی برای آلزایمر وجود ندارد، اگرچه داروهایی وجود دارند که می توانند علائم این بیماری را درمان کنند.
نورکسین ها
نورکسین ها (Nrxns) خانواده بزرگی از پروتئین های چسبنده پیش سیناپسی را تشکیل می دهند. آزادسازی انتقال دهنده های عصبی و تعاملات ترانس سیناپسی را با لیگاندهای پس سیناپسی جفت می کنند. مطالعات ژنتیکی و تجزیه و تحلیل پروتئین ها در نمونههای محیطی بیماران، نقشی را برای سطوح تغییر یافته Nrxn در مراحل پیش بالینی و بالینی بیماری آلزایمر (AD) نشان میدهد. Nrxns در سطوح مختلف تنظیم می شوند. در سطح رونویسی، استفاده از پروموترهای جایگزین همراه با پیوند گسترده جایگزین صدها ایزوفرم را ایجاد می کند. اینها در حوزه خارج سلولی متفاوت هستند. برش پروتئولیتیک به عنوان یک مکانیسم جدید پس از ترجمه عملکرد Nrxn را تنظیم می کند. تنظیم پروتئولیتیک Nrxns در دو مرحله متوالی انجام می شود. ابتدا، یک شکاف در ناحیه مجاور غشاء، اکتودومین خاص ایزوفرم پردازش شده را آزاد می کند. سپس قطعه C ترمینال Nrxn متصل به غشاء (NrxnCTF) ایجاد می کند.
متعاقباً، NrxnCTF توسط Presenilins (PS)، زیرواحد فعال کمپلکس گاما سکرتاز، پاکسازی می شود.
گاما سکرتاز واسطه برش درون غشایی تعدادی از ماتریکس ها است. نکته مهم، جهش در ژنهای PSEN1/2 علت اصلی AD خانوادگی (fAD) است. که حدود 90 درصد موارد fAD را توضیح میدهد. چندین یافته تأیید می کند که جهش های PSEN مرتبط با fAD از طریق مکانیسم از دست دادن عملکرد عمل می کنند. نشان داده شد که موشهای فاقد ژن PS1/2 در نورونهای بالغ، علائم کلیدی شبیه آلزایمر داشتند. علائم شامل نقص اولیه و پیشرونده در شکلپذیری سیناپسی و حافظه بود. همچنین به دنبال آن از دست دادن دیررس سیناپس، تخریب عصبی و هیپرفسفریلاسیون پروتئین های تائو را نیز نشان میدهند.
به این ترتیب، از دست دادن عملکرد PS منجر به کاهش فعالیت گاما-سکرتاز می شود.
درنتیجه باعث تجمع لایه های پروتئولیتیک آن به شیوه ای وابسته به ماتریکس می شود. بنابراین، تجمع یک بستر خاص همزمان با شروع علائم به تعیین نامزدهای بالقوه مرتبط با اختلال عملکرد PS کمک می کند. با این حال، تعداد بالای سوبستراها برای PS / گاما-سکرتاز شناسایی کاندیدهای منفرد با ارتباط عملکردی در از دست دادن عملکرد PS را به چالش می کشد. بنابراین، بسترهای PS/گاما-سکرتاز که میتوانند نقصهای کلیدی سیناپسی و حافظه مرتبط با از دست دادن عملکرد PS را ایجاد کنند، کاملاً شناخته شده نیستند.
خلاصه مطالعه
یافته ها نشان می دهد که تجمع پروتئین سیناپسی نورکسین ممکن است یکی از دلایل از دست دادن حافظه مرتبط با بیماری آلزایمر باشد. اعضای گروه “اختلال و بیماری سیناپسی” در موسسه زیست پزشکی سویل (IBiS)، به رهبری محققان فرانسیسکو گومز شول و آمالیا مارتینز میر، اخیراً نتایج تحقیقات خود را در مورد بیماری آلزایمر منتشر کردند. دادههای بهدستآمده نشان میدهد که تجمع بخشی از پروتئین سیناپسی نورکسین در مغز بزرگسالان باعث از دست دادن حافظه خاص میشود. این کار با همکاری گروهی به رهبری خوزه ماریا دلگادو گارسیا در بخش علوم اعصاب دانشگاه پابلو دو اولاوید انجام شد.
این مشارکت یک مرحله مقدماتی در مطالعه پروتئین در نمونه های بیماران بود.
مطالعات رفتاری
سوبسترای نورکسین برای پرسنیلین در مغز قدامی بزرگسالان به صورت انتخابی بیان می شود. باعث نقص در حافظه مشارکتی و شکل پذیری پیش سیناپسی می شود.
پرسنیلین ها (PS) زیرواحد فعال کمپلکس گاما سکرتاز را تشکیل می دهند. واسطه پاکسازی پروتئولیتیک طیف وسیعی از پروتئین های غشای پلاسمایی نوع I است. جهش های از دست دادن عملکرد در ژن های PSEN1/2 علت اصلی بیماری آلزایمر خانوادگی (fAD) است. با این حال، سوبستراهای PS/gama-secretase مربوط به نقصهای عصبی مرتبط با از دست دادن عملکرد PS کاملاً شناخته شده نیستند.
این مطالعه

درباره نویسنده
خجسته رحیمی جابری، پژوهشگر دکترای تخصصی علوم اعصاب دانشگاه علوم پزشکی شیراز و نویسنده وب سایت انستیتو سلامت مغز دانا. زمینه کاری تخصصی ایشان مشکلات حافظه و آلزایمر است وی بیش از 20 مقاله معتبر بین المللی در این زمینه به چاپ رسانده است. می توانید پژوهش های او را در اینجا (کلیک کنید) دنبال کنید.