- تومور مغزی چیست؟
- انواع تومورهای مغزی
- تبدیل سلول های گلیوما به سلول های عصبی ممکن است تومورهای مغزی از نوع گلیوبلاستوما را درمان کند.
- تومورهای مغزی GBM
- روش مطالعه
- الگوهای بیان ژنی
- شرایط in vivo
- پروفسور چن در پایان می گوید:
- خلاصه مطالعه
- نتایج
- نتیجه گیری کلی
- برای اطلاع از درمان های جدید در زمینه بیماریهای سیستم عصبی، با ما در مرکز سلامت مغز دانا در تماس باشید.
- درباره نویسنده
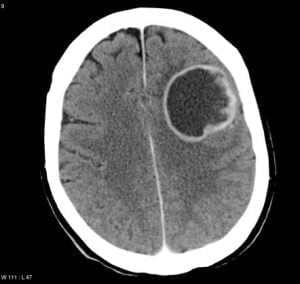
تومور مغزی چیست؟
تومور مغزی مجموعه یا توده ای از سلول های غیر طبیعی در مغز است. جمجمه مغز را در بر می گیرد، بسیار سفت و سخت است. هر گونه رشد در چنین فضای محدودی می تواند مشکلاتی ایجاد کند. تومورهای مغزی می توانند سرطانی (بدخیم) یا غیر سرطانی (خوش خیم) باشند. هنگامی که تومورهای خوش خیم یا بدخیم رشد می کنند، می توانند باعث افزایش فشار داخل جمجمه شوند. این می تواند باعث آسیب مغزی شود و می تواند تهدید کننده زندگی باشد. تومورهای مغزی به دو دسته اولیه یا ثانویه تقسیم می شوند. تومور مغزی اولیه از مغز شما منشا می گیرد. بسیاری از تومورهای اولیه مغزی خوش خیم هستند. تومور مغزی ثانویه به عنوان تومور متاستاتیک مغز نیز شناخته میشود. زمانی که سلولهای سرطانی از اندام دیگری مانند ریه یا سینه به مغز گسترش مییابند.
انواع تومورهای مغزی
تومورهای مغزی اولیه
تومورهای مغزی اولیه از مغز منشا می گیرند. آنها می توانند از طریق موارد متعددی ایجاد شوند. غشاهایی که مغز را احاطه کرده اند که به آنها مننژ می گویند. سلول های عصبی غدد تومورهای اولیه می توانند خوش خیم یا سرطانی باشند. در بزرگسالان، شایع ترین انواع تومورهای مغزی گلیوما و مننژیوم هستند.
تومورهای مغزی ثانویه
تومورهای ثانویه مغزی اکثریت سرطان های مغز را تشکیل می دهند. آنها از یک قسمت از بدن شروع می شوند و به مغز گسترش می یابند یا متاستاز می کنند. سرطان ریه، سرطان پستان، سرطان کلیه، سرطان پوست، که می توانند به مغز گسترش یابند. تومورهای ثانویه مغزی همیشه بدخیم هستند. تومورهای خوش خیم از یک قسمت بدن به قسمت دیگر منتقل نمی شوند.
تبدیل سلول های گلیوما به سلول های عصبی ممکن است تومورهای مغزی از نوع گلیوبلاستوما را درمان کند.
گلیوما از شایع ترین تومورهای اولیه مغزی در بزرگسالان است. در میان آنها، گلیوبلاستوما با درجه بالا (GBM) بسیار شناخته شده است و به شدت تهاجمی است. علاوه بر تهاجمی بودن، پزشکان در درمان آنها نیز با چالش های زیادی مواجه اند. این بیماری در مدت زمان کوتاهی به سرعت به مرحله پیشرفته می رسد. معمولا بقای چنین بیمارانی اغلب مأیوس کننده است. درمان های هدفمندی که می تواند میزان بقا و کیفیت زندگی بیماران مبتلا به GBM را به طور معنی داری بهبود بخشد، وجود ندارد. درمان های فعلی بر مهار رشد تومور یا از بین بردن سلول های سرطانی متمرکز شده است. با این حال، با توجه به سازگاری بالا، مقاومت و تنوع این تومورها، چنین درمان هایی به تنهایی کافی نیست.
تومورهای مغزی GBM
GBM ها ناشی از تقسیم بی رویه سلول های گلیال هستند. همانطور که می دانید، گلیال ها، سلول های عصبی را تغذیه کرده و ماتریس حمایتی بافت مغز را تشکیل می دهند. بر خلاف سلول های عصبی که تقسیم نمی شوند، سلول های گلیال می توانند تحت تقسیم سلولی قرار بگیرند. بنابراین همین امر آنها را مستعد تشکیل تومور می کند. محققان دانشگاه ایالتی پنسیلوانیا، ایالات متحده و دانشگاه جینان، با بهره گیری از این تمایز بین دو نوع سلول، اکنون یک استراتژی جدید کشف کرده اند. روشی که با برنامه ریزی مجدد، سلول های گلیوما تکثیر کننده را به نورون های غیر تکثیر کننده تمایز می دهد.
پروفسور گونگ چن، دانشمند ارشد و نویسنده مقاله است. نتایج کار آنها در Cancer Biology & Medicine منتشر شده است. “استراتژی برنامه ریزی مجدد ما اساساً با سایر درمان های ضد سرطان متفاوت است. هدف ما کشتن سلول های گلیوما نیست. بلکه ما می خواهیم آنها را به نورون ها تبدیل می کنیم. بنابراین، عوارض جانبی بالقوه این درمان، بر روی سایر سلول های طبیعی کم است”.
روش مطالعه
ما با برنامه ریزی مجدد، سلول های گلیوما را در شرایط in vitro و in vivo، با استفاده از عوامل رونویسی عصبی، به سلول های عصبی تبدیل کردیم.”
سلول های گلیوما با برنامه ریزی مجدد، بیشتر شبیه نورون ها شده و نشانگرهای خاصی برای سلول های عصبی تولید می کنند. این تغییر هویت به نورون ها، میزان تقسیم (یا تکثیر) آنها را به میزان قابل توجهی کاهش داد. محققان دریافتند که هر یک از عوامل رونویسی عصبی، باعث تبدیل سلول به یک نوع سول عصبی متفاوتی می شود. بیان Neurog2 سریع ترین و کارآمدترین رویکرد تبدیل سلول را به همراه داشت. بر اساس انتقال دهنده عصبی منتشر شده، اکثر سلول های بیان کننده Neurog2 و NeuroD1 به نورون های گلوتاماترژیک تبدیل شدند. در حالی که سلول های بیان کننده Ascl1 به نورون های GABAergic (گاباارژیک) تبدیل شدند و بر تأثیرات سیگنالینگ خاص هر عامل تأکید کردند.
الگوهای بیان ژنی
این تفاوت ها همچنین با الگوهای بیان ژن متمایز در زیرگروه های مختلف عصبی همراه بود. نتایج تجزیه و تحلیل توالی RNA این الگوهای بیان ژن متمایز را نشان داد. از تکنیک توالی یابی RNA، برای مطالعه ژن های بیان شده متفاوت استفاده می شود. در مرحله بعد، آنها سلول های گلیوما را از نظر ویژگی های سلولی و عملکردی آنها ارزیابی کردند. این سلول های تبدیل شده، آرایش اندامک درون سلولی مشابه نورون ها را نشان دادند. همچنین فعالیت انتقال سیگنال عصبی را نیز تا حدودی بروز دادند.
شرایط in vivo
در شرایط in vivo، محققان رتروویروس هایی را بیان کردند که عوامل فوق را به مغز موش های پیوند شده با سلول های GBM تزریق کردند. سلول های GBM به طور موثر به سلول های عصبی در موش تبدیل شدند، که با نشانگرهای زیستی عصبی مشخص می شوند. علاوه بر این، دگرگونی سلولی نیز به طور قابل توجهی از تکثیر این سلول ها در مدل های حیوانی جلوگیری می کند. در مجموع، این یافته ها نشان می دهد که برنامه ریزی مجدد سلولی، یک استراتژی درمانی امیدوار کننده برای کند کردن یا توقف رشد GBM بود. در این رویکرد، عوارض جانبی مضر درمان های معمول ضد سرطان بر روی سلول های سالم مغز حذف شد.
پروفسور چن در پایان می گوید:
“مطالعه ما مسیر جدیدی را برای جلوگیری از رشد گلیوما باز می کند. مطالعات آینده ای که از جوندگان به نخستی های غیر انسانی منتقل می شود، به آزمایش این امر کمک می کند. بررسی اینکه آیا می توانیم از این استراتژی برنامه ریزی مجدد برای درمان گلیومای بزرگ در مغز میمون استفاده کنیم یا خیر. در صورت موفقیت، درمان امیدوار کننده ای برای میلیون ها بیمار مبتلا به گلیوما در سراسر جهان ارائه می دهد. ”
تغییر سرنوشت سلول ها در واقع ممکن است سرنوشت بیماران GBM را نیز دگرگون کند!
خلاصه مطالعه
هدف: گلیوبلاستوما (GBM) از شایع ترین و تهاجمی ترین تومورهای مغزی در سیستم عصبی بزرگسالان است. رویکردهای درمانی برای درمان GBM تحت بررسی شدید، از جمله استفاده از ایمونوتراپی های نوظهور است. در اینجا، ما برنامه ریزی مجدد سلول های تکثیر کننده GBM به نورون های غیر تکثیر کننده پیشنهاد می کنیم.
روش ها: در اینجا از رتروویروس ها برای هدف قرار دادن سلول های GBM انسانی از طریق تکثیر بیش از حد فاکتورهای رونویسی عصبی استفاده شد. از رنگ آمیزی سیستم ایمنی، ضبط الکتروفیزیولوژیکی و ارزیابی توالی های RNA انبوه، استفاده کردیم. درواقع مکانیسم های ضد تغییر سلول های GBM انسان را بررسی کردیم. یک مدل موش زنوگرافت داخل جمجمه ای، برای بررسی تبدیل عصبی سلولهای GBM انسان مورد استفاده قرار گرفت.
نتایج
ما با بیان بیش از حد فاکتور رونویسی، تمایز عصبی ای موثری از سلول های GBM انسان را گزارش می دهیم. فاکتورهای مختلف نیز شامل فاکتور تمایز دهنده -1 (NeuroD1)، نوروژنین -2 (Neurog2)، یا Achaete-scute 1 (Ascl1) بودند. ارزیابی خصوصیات انواع نورون ها نشان داد که اکثر نورون های تبدیل شده با کمک Neurog2 و NeuroD1 از نوع گلوتاماتژیک هستند. در حالی که Ascl1 به نفع سلول های گاباارژیک بود. نورون های تبدیل شده به سلول GBM نه تنها نشانگرهای pan-neuronal را نشان می دهند بلکه فعالیت های الکتروفیزیولوژیکی مشخصه نورون را نیز نشان می دهند.
تجزیه و تحلیل فرایند رونویسی نشان داد که ژن های عصبی در سلول های گلیوما پس از بیان بیش از حد عوامل رونویسی عصبی فعال می شوند. متعاقبا مسیرهای مختلف پیام رسانی توسط عوامل مختلف رونویسی عصبی فعال می گردد. نکته مهم این است که تبدیل عصبی سلول های GBM با مهار قابل توجه تکثیر سلول GBM در هر دو مدل in vitro و in vivo همراه بود.
نتیجه گیری کلی
این نتایج نشان می دهد که سلول های GBM را می توان در زیرگروه های مختلف نورونی برنامه ریزی کرد. این امر منجر به یک رویکرد جایگزین قوی برای درمان تومورهای مغزی با استفاده از فناوری تبدیل سلول در داخل بدن می شود.
برای اطلاع از درمان های جدید در زمینه بیماریهای سیستم عصبی، با ما در مرکز سلامت مغز دانا در تماس باشید.
منبع: https://neurosciencenews.com/glioma-glioblastoma-cancer-19331/