تحقیقات جدیدی که در دانشگاه شیکاگو انجام شد نشان داد که در مدلی از بیماری آلزایمرکه در موشهای نر صورت گرفت، بین میکروگلیاها (سلولهای ایمنی مغز) و میکروبیوم روده و همچنین رسوبات بتا-آمیلوئید ، ارتباطی وجود دارد.
مطالعه ای در 2 دسامبر در مجله Experimental Medicine منتشر شد. نتایج نشان داد که سلولهای ایمنی مغز با میکروبهای روده در ارتباط هستند. این ارتباط ممکن است هدف مهمی برای پیشگیری و درمان بیماری زوال عقل در بیماران انسانی باشد.
میکروبیوم های روده چیست؟
میکروبیومهای روده میکروارگانیسمهایی از جمله باکتریها و یوکاریوتهای میکروسکوپی هستند. این میکروبیومها در دستگاه گوارش انسان و سایر حیوانات از جمله حشرات زندگی میکنند. اصطلاحات جایگزین شامل فلور روده و یا میکروبیوتای روده می باشد. متاژنوم دستگاه گوارش (گاهی اوقات به عنوان میکروبیوم تعریف می شود) مجموعه ای از تمام ژنوم میکروبیومهای روده است. روده محل اصلی میکروبیومهای انسان است. میکروبیومهای روده تأثیرات گسترده ای بر بدن دارند. از جمله تأثیر بر مقاومت در برابر کلونیزاسیون در برابر عوامل بیماری زا، حفظ اپیتلیوم روده، متابولیسم ترکیبات غذایی و دارویی، کنترل عملکرد ایمنی، و حتی رفتار از طریق محور روده-مغز.
این مطالعه که مبتنی بر تحقیقات قبلی است، نشان میدهد در اوایل زندگی براثر درمان با آنتیبیوتیکها، میکروبیوم های روده ممکن است دچار اختلال شوند. این مورد برخی از علائم بارز بیماری آلزایمر (AD) را در موشهای سوری نر کاهش می دهد، اما در موشهای سوری ماده چنین اثری مشاهده نشد.
Sangram Sisodia، نویسنده مطالعه بیان کرد:
در مطالعات قبلی ما به موش ها بلافاصله پس از تولد آنتی بیوتیک دادیم. تجویز آنتی بیوتیک به موشها باعث کاهش رسوب آمیلوئید در آنها شد. این کاهش به طور خاص در حیوانات نر که مدل خاصی از بیماری آلزایمر در آنها ایجاد شده بود مشاهده گردید.
از طرفی ما زیستشناسی میکروگلیاها را در مغز بررسی کردیم. ما دریافتیم که در حیوانات نر، تغییرات قابلتوجهی در بیان ژن و مورفولوژی سلولها وجود دارد. بنابراین در این مطالعه، ما تصمیم گرفتیم میکروگلیا را به طور خاص در چارچوب این الگو بررسی نماییم.
این مطالعه با استفاده از موشهای APPPS1-21، یک مدل ژنتیکی پرکاربرد در AD انجام شد. این حیوانات آسیب شناسی های مرتبط با AD را ایجاد می کنند. از جمله دارای پلاک های آمیلوئیدی هستند، که تصور می شود نقش مهمی در وضعیت تخریب سلولهای عصبی دارند. برخلاف مطالعه گذشته، مطالعه جدید مستلزم درمان موشها با آنتیبیوتیک به مدت یک هفته در اوایل زندگی آنها بود. حتی با چنین درمان کوتاهی، محققان شاهد کاهش چشمگیر در سطح آمیلوئید بتا در مغز موشهای نر در سن 9 هفتگی بودند. نکته مهم این است که موش های ماده چنین تفاوتی را نشان ندادند.
بدن انسان حاوی تریلیون ها سلول باکتری است. این جامعه باکتریایی وسیع و عمدتا ناشناخته که به عنوان میکروبیوم شناخته می شود، با بسیاری از جنبه های سلامت انسان، از بیماری های گوارشی گرفته تا چاقی، مرتبط است. مختل کردن میکروبیوم با آنتیبیوتیکها، با از بین بردن باکتریهای مفید در روده ما میتواند باعث بیماری شود.
بازیابی میکروبیومهای موشها، قبل از دریافت آنتی بیوتیک با روش FMT، پلاک های آمیلوئیدبتا را به طور کامل ترمیم کرد. گویی موش ها هرگز در معرض آنتی بیوتیک ها قرار نگرفته بودند. علاوه بر این، میکروگلیاهای محافظ عصبی در موشهای نر تحت درمان با آنتیبیوتیک به میکروگلیای تخریب کننده عصبی با FMT تبدیل شدند. این شرایط مشابه وقتی است که موشها اصلا در معرض آنتیبیوتیکها قرار نگرفته باشند.
Sisodia بیان کرد: «میکروگلیاها حافظه دارند. ما دقیقاً نمی دانیم این حافظه چیست. اما می دانیم که آنها می توانند با تغییر شکل و بیان ژن خود به یک پاتوژن یا اختلال پاسخ دهند. آنها همچنین می توانند آن تغییرات را برای مدت طولانی حفظ کنند.
آنچه ما در این مطالعه می بینیم این است که پس از درمان آنتی بیوتیکی در اوایل زندگی، رسوب آمیلوئید به طور قابل توجهی در موشهای نر کاهش می یابد و این تغییر در موشهای ماده دیده نمی شود. ما می بینیم که رونوشت میکروگلیال (بیان ژن آنها) نیز تغییر کرده است. اما اگر باکتری های موجود در مدفوع موش های درمان نشده را به موش های تحت درمان با آنتی بیوتیک پیوند دهند، آسیب شناسی و همچنین فنوتیپ میکروگلیال بازیابی می شود.
سوال آخر این است که آیا میکروگلیا مسئول آمیلوئیدوز (بیماری که در آن پروتئینهای آمیلوئید در اندامها و بافتها انباشته میشوند) است؟ اگر چنین است، میکروگلیا چگونه این کار را انجام می دهد؟
برای پاسخ به این سوال، محققان دارویی به نام PLX5622 را به موش ها دادند. این دارو میکروگلیای مغز موش و همچنین برخی از سلول های ایمنی محیطی در جریان خون را از بین می برد. آنها دریافتند که بدون میکروگلیا، درمان آنتی بیوتیکی هیچ تاثیری بر آمیلوئیدوز در مغز ندارد. بنابراین میکروگلیا برای واسطه این اثر حیاتی است.
Dodiya نویسنده اول این مطالعه گفت: «در واقع، این مطالعه سه چیز کلیدی را به ما نشان میدهد. اولین مورد، تفاوتهای جنسیتی در آمیلوئیدوز مغز پس از اختلالات اولیه در میکروبیوم روده در اوایل زندگی افراد است. مورد دوم این است که انجام پیوند مدفوع پس از درمان آنتی بیوتیکی باعث بازگرداندن آمیلوئیدوز میشود. سوم اینکه میکروگلیا عامل مهمی است که باعث تغییرات ایجاد شده توسط میکروبیوم می شود.
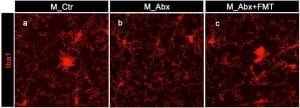
میکروگلیا در مغز موشهای نر مبتلا به بیماری آلزایمر که به دلیل داشتن پلاکهای بتا آمیلوئید،دچار تخریب عصبی شده اند (سمت چپ). در حالی که درمان موشها با آنتیبیوتیکها در اوایل زندگی منجر به نمایش میکروگلیا به عنوان «عامل محافظ عصبی» شده است. آمیلوئیدوز نیز در این شرایط کاهش یافته است. اثرات مفید آنتی بیوتیک ها را می توان با پیوند ساده مدفوع (سمت راست) معکوس کرد.
هدف این تیم تحقیقاتی چیست؟
تیم تحقیقاتی در حال انجام مطالعات بیشتری هستند که میکروگلیا را مستقیمتر مورد هدف قرار دهند. آنها میخواهند اطمینان حاصل شود که اثرات PLX5622 بر سلولهای ایمنی ذاتی بدن بر آمیلوئیدوز در مغز تأثیر نمیگذارد. آنها امیدوارند که مشخص کنند روده چه سیگنال هایی به مغز می فرستد که منجر به این تغییرات در میکروگلیا می شود. همچنین چگونه میتواند به نوبه خود منجر به تغییرات در پلاک های آمیلوئید شود.
این تیم همچنین در حال بررسی این سوال است که چرا این اثرات فقط در موش های نر دیده می شود؟!!
Sisodia گفت: «این یک اثر خیره کننده است. به نظر می رسد در جنس ماده، میکروگلیا به هیچ وجه تحت تأثیر اختلالات میکروبیوم قرار نمی گیرد. تحقیقات در گذشته نشان داده است که میکروگلیا حیوانات نر و ماده در طول رشد و پیری بسیار متفاوت است. اما چه عواملی در ایجاد آن نقش دارند؟ احتمالاً این اثر در نتیجه هورمون های جنسی است. اما آنها چه تأثیراتی بر میکروبیوم دارد؟
روشن کردن این سوال می تواند برای درمان AD در بیماران انسانی مهم باشد. Sisodia گفت: زنان نسبت به مردان در معرض خطر بیشتری برای ابتلا به آلزایمر هستند. اگر ما میدانستیم که چه مولکول هایی در این زمینه نقش ایفا میکنند، بیماری معمولا زودتر تشخیص داده می شد. شاید در آینده بتوانیم در مورد چگونگی هدف قرار دادن این بیماری و اینکه چرا این تفاوت ها را بین مردان و زنان مشاهده می کنیم، پاسخ بهتری پیدا کنیم.
برای کسب اطلاعات بیشتر به سایت سلامت مغز دانا مراجعه نمایید.