خلاصهی کاربردی: TMS با ایجاد یک میدان مغناطیسی گذرا، جریانهای الکتریکی بسیار کوچک در قشر مغز القا میکند و از مسیر «پلاستیسیتی» شبکههای عصبی را تعدیل میکند. فرکانسهای پایینتر معمولاً اثری (مشابه LTD) و فرکانسهای بالاتر یا iTBS اثر تحریکی (مشابه LTP) دارند.
- از یک ایده مهندسی تا درمانهای بالینی
- چرا این تاریخچه مهم است؟
- مسیر تکامل تا امروز؛ چه آموختیم؟
- فیزیک TMS (تحریک مغناطیسی فراجمجمهای)
- 1) از قانون فاراده تا پالس TMS
- Double-cone coil
- H-coil (BrainSway)
- فیزیولوژی TMS (روان و کاربردی)
- نکات بالینی سریع (ترجمهٔ فیزیولوژی به اجرا)
- «TMS دقیقاً چه میکند؟» (ساده و کاربردی)
- «آنلاین» در برابر «آفلاین»
- تکپالس بهعنوان ابزار پیشبالینیِ دقیق
- از «پالس» تا «پلاستیسیته»
- چه زمانی از هرکدام استفاده کنیم؟
- ایمنی و دوزینگ در عمل (rTMS/TBS)
- عوارض شایع و اقدامات کاهش ریسک
- 3) چارچوب کلی دوزینگ (بدون بازی با پارامترها!)
- رویهها و نقشها در کلینیک
- هدفگیری و لوکالیزیشن (کجا و چگونه کویل را بگذاریم؟)
- چرا لوکالیزیشن اینقدر مهم است؟
- روشهای رایج لوکالیزیشن DLPFC (افسردگی)
- زاویهٔ کویل و جهت E-Field
- عمق و فاصلهٔ پوست–قشر (SCD)
- چکلیست «جلسهٔ اول» (لوکالیزیشن و مستندسازی)
- نگهداری تکرارپذیری در جلسات بعدی
- هدفگیری در اندیکاسیونهای دیگر (خیلی خلاصه)
- اشتباهات متداول و راهحل
- انتخاب پروتکل بر پایهٔ تشخیص (Clinical Indication → Target & Protocol)
- فلوچارت عملی دورهٔ درمان (از پذیرش تا پایان و نگهدارنده)
- همزمانی با دارو/رواندرمانی و مدیریت عوارض حین درمان
- پاسخ، رمیسیون، بوستر/نگهدارنده و «الگوریتم عدمپاسخ» (کاملاً اجرایی)
- مستندسازی، رضایت آگاهانه، SOP و مدیریت کیفیت در درمان rTMS
- پایش پاسخ، پیشبینیکنندهها و مدیریت «عدمپاسخ» در rTMS
- ایمنی، عوارض شایع و مدیریت آنها در rTMS
- سفارشیسازی پروتکلها برای اختلالات مختلف
- جمعیتهای خاص، احتیاطات تخصصی + SOP و «رضایت آگاهانه» کوتاه rTMS
- برنامه «بوستر/نگهدارنده» پس از rTMS + Recall و پیگیری ۳–۶ ماهه + فرم خروج یکصفحهای
از یک ایده مهندسی تا درمانهای بالینی
داستان TMS از شفیلد انگلستان شروع شد؛ جایی که گروهی از مهندسان در ابتدا قصد ساخت «تحریککننده عصب محیطی» را داشتند و اصلاً هدفشان تحریک مغز نبود. اما همانجا «جرقهٔ ایده»ی استفاده از میدان مغناطیسی برای تحریک غیرتهاجمی مغز زده شد و در سال ۱۹۸۵ نخستین دستگاه مدرن TMS معرفی گردید—و بقیه، تاریخ است.
نکتهٔ کلیدی: «تولد تصادفی» TMS از دل مهندسی اعصاب محیطی، مسیر تازهای در نورومدولاسیون گشود و در کمتر از چند دهه به ابزار استاندارد پژوهشی و درمانی تبدیل شد.
چرا این تاریخچه مهم است؟
ریشهٔ بینرشتهای: خاستگاهِ کاملاً مهندسی بههمراه پذیرش سریع در علوم اعصاب، باعث شد TMS خیلی زود هم در تحقیق و هم در درمان جا بیفتد.
بلوغ سریع پروتکلها: از همان سالهای نخست، پروتکلهای متنوع (پالستک، جفتپالس، rTMS، تتابرس) و کاربردهای پژوهشی/بالینی بهسرعت توسعه یافتند.
مسیر تکامل تا امروز؛ چه آموختیم؟
از «کشف» تا «استانداردسازی»: معرفی دستگاه در ۱۹۸۵ آغاز راه بود؛ اما آنچه TMS را ماندگار کرد، استانداردسازی تدریجی پروتکلها و ایمنی آن در پژوهش و درمان بود.
جایگاه کنونی: امروز TMS یک فناوری غیرتهاجمی، مبتنیبر فیزیک میدانهای متغیر و قابل تکرار است که در کنار تصویربرداری و آزمونهای عصبروانشناختی، به ستون سومِ نورومدولاسیون بالینی تبدیل شده است.
فیزیک TMS (تحریک مغناطیسی فراجمجمهای)
1) از قانون فاراده تا پالس TMS
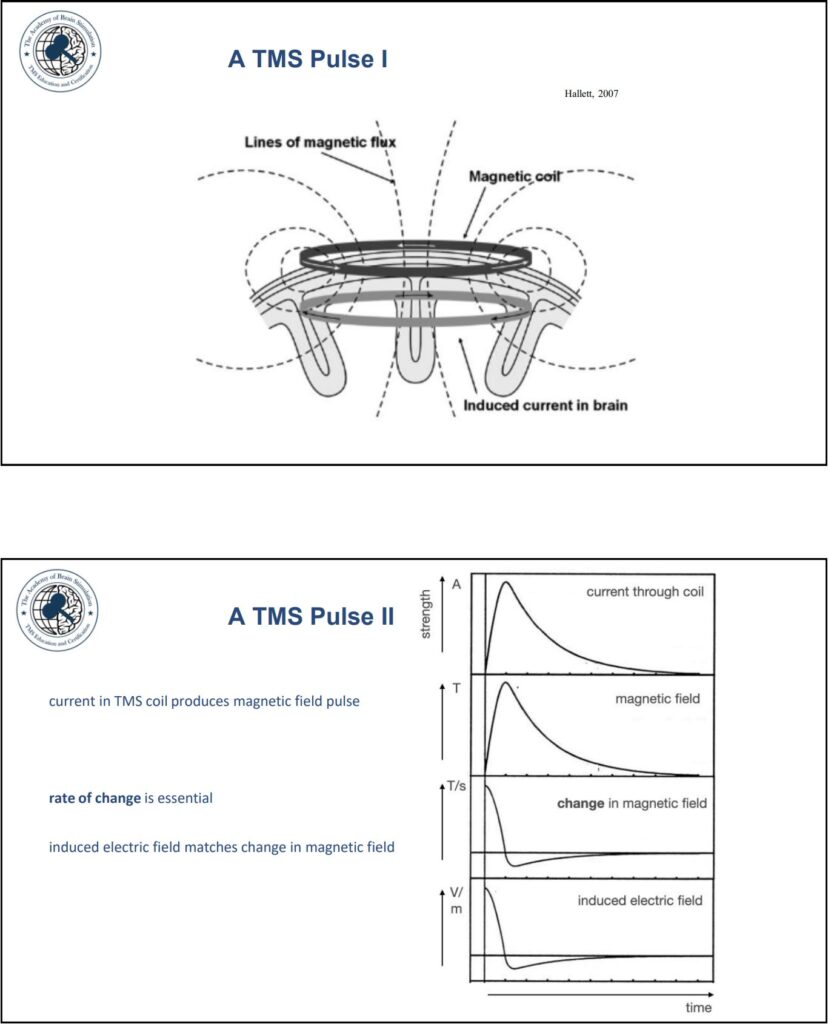
اصل فیزیکی: وقتی جریانِ لحظهای از کویل TMS عبور میکند، یک پالس میدان مغناطیسی ایجاد میشود. طبق قانون فاراده/معادلهٔ مکسول–فاراده، هر میدان مغناطیسیِ متغیر با زمان، یک میدان الکتریکیِ القایی در فضای پیرامون (از جمله قشر مغز) ایجاد میکند؛ همان میدانی که نورونها را تحتتأثیر قرار میدهد.
- نرخ تغییر میدان مهمتر از «قدر مطلق» است: «قدرت تحریک» بهطور انتقادی به dB/dt (نرخ تغییر میدان) وابسته است؛ پالسهای کویل هرچه تندتر تغییر کنند، میدان الکتریکی القایی قویتری در بافت تولید میشود.
- سختافزار در یک خط: «یک کلید مدار را میبندد → جریان از کویل میگذرد → پالس میدان مغناطیسی ایجاد میشود.»
نتیجهٔ عملی: طراحی پالس و الکترونیک تغذیه، طوری بهینه میشود که dB/dt بالا و تکرارپذیر بهدست آید؛ این همان چیزیست که پالس TMS را «نورون-موثر» میکند.
2) کاهش شدت با فاصله و «چرا عمدتاً قشر؟»
شدت اثر TMS با فاصله از کویل بهسرعت کاهش مییابد؛ به همین دلیل تحریک مؤثر، عملاً به لایههای قشری و زیرقشریِ کمعمق محدود میشود (در دستگاههای استانداردِ سطحی).
3) هندسهٔ کویل، فوکالیتی و عمق
الف) فیگور–۸ (Butterfly/Figure-of-Eight)
فوکالترین انتخاب استاندارد: کویل فیگور–۸ کانونیترین الگوی میدان را میدهد و برای بیشترین پروتکلهای قشری (مثل DLPFC) انتخاب اول است. «قاعدهٔ سرانگشتیِ سطح اثر» در منابع کلاسیک حدود ۱ سانتیمتر مربع بیان میشود (وابسته به شدت). همچنین خود شدت هم روی فوکالیتی اثرگذار است.
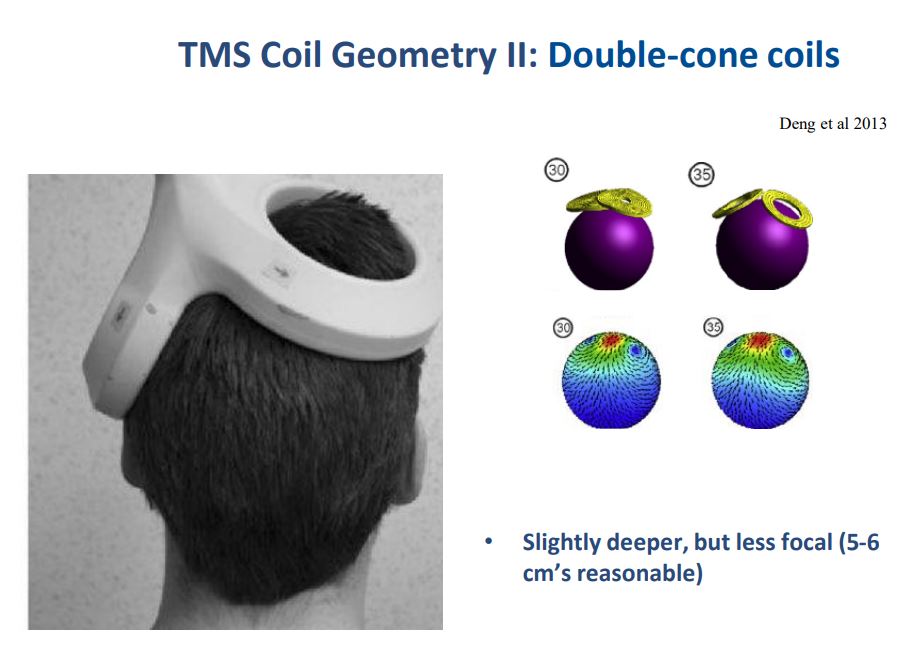
ب) دابل–کُن (Double-Cone)
کمی عمیقتر، اما کمکانونتر: برای اهدافی که نیاز به نفوذ بیشتر دارند (مثلاً نواحی میانی–خطمیانی)، دابل–کُن عمق مؤثر بیشتری میدهد ولی فوکالیتی کاهش مییابد؛ عمق معقول حدود ۵–۶ سانتیمتر ذکر شده است. همچنین بهدلیل ترکیب چند حلقه/جهت میدانی، افت شدت با عمق کندتر و در عوض تحریک سطحی کمتر میشود.
پ) H-Coil (Deep TMS)
تحریک عمیقتر شبکهها: آرایش ویژه حلقهها در H-coil باعث میشود میدان اهداف عمیقتر در دسترس قرار گیرند (با بهای کاهش کانونیّت سطحی).
جمعبندی هندسه: «فیگور–۸» = کانونی و انتخاب غالب برای قشر؛ «دابل–کُن/H-coil» = نفوذ بیشتر با کاهش کانونیّت سطحی. در انتخاب، هدف بالینی و آناتومی فرد تعیینکننده است.
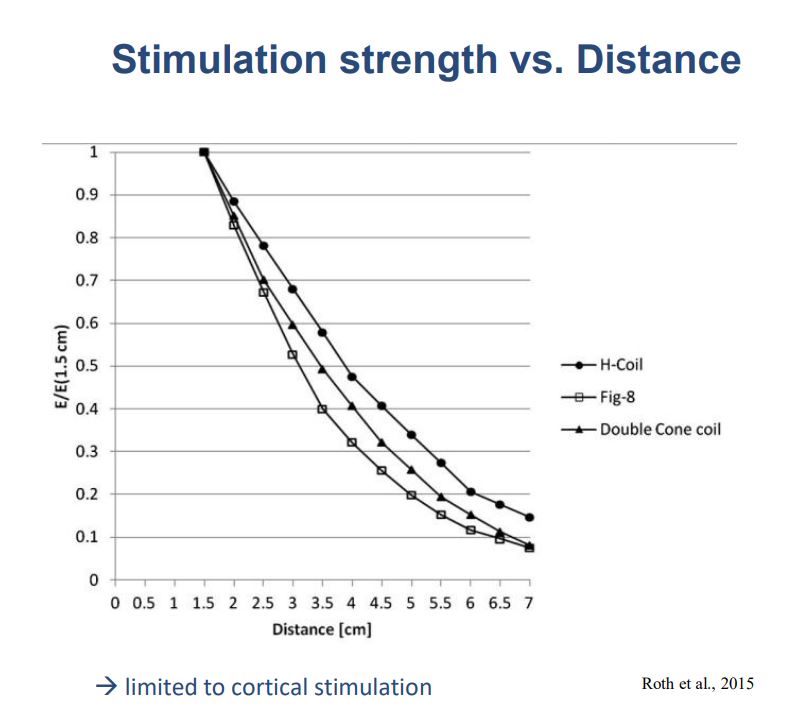
قدرت تحریک در برابر فاصله (Stimulation strength vs. Distance)
این نمودار نشان میدهد میدان الکتریکیِ القایی TMS وقتی از سطح کویل دور میشویم خیلی سریع افت میکند. محور افقی فاصله از کویل (cm) و محور عمودی نسبتِ شدت میدان به مقدار آن در عمق ۱.۵ سانتیمتری است E/E(1.5cm)E/E(1.5 cm). سه منحنی برای سه نوع کویل هستند:
Fig-8 (شکلِ هشت): بیشترین تمرکز (focality) را دارد ولی با افزایش فاصله سریعتر افت میکند.
Double-cone: نفوذ کمی بیشتر از شکلِ هشت، اما کمتر متمرکز.
H-coil (Deep TMS): در فاصلههای بیشتر افتِ کمتری دارد، یعنی نفوذ عمقیتر ایجاد میکند، گرچه همچنان شیب کاهش زیاد است.
برداشتهای عددی تقریبی از نمودار
حوالی ۳ cm: میدان القایی برای شکلِ هشت ≈ ۴۰%، دابلکون ≈ ۵۰%، و H-coil ≈ ۶۰–۷۰% مقدارِ مرجع است.
حوالی ۵ cm: به حدود ۱۵–۳۰% میرسد.
حوالی ۶–۷ cm: نزدیک ۱۰% یا کمتر.
پیام بالینی
چرا TMS «قشری» است؟ چون بهدلیل افت شدید با فاصله، تحریک مؤثر عمدتاً به قشرِ مخ محدود میشود؛ برای ساختارهای عمقی، حتی با H-coil هم میدان در عمق زیاد ضعیف و گسترده است (فوکوس کمتر).
فاصله پوست تا قشر (SCD) مهم است: هرچه SCD بیشتر، برای رسیدن به همان E-field باید % قدرت دستگاه را بالاتر ببرید (دوزینگ مبتنی بر آستانه حرکتی یا مدلسازی E-field/اصلاح SCD توصیه میشود).
برای کاهش فاصله مؤثر و پایدارسازی دوز:
تماس محکم و یکنواخت کویل با سر (موهای پفدار/کلاه ضخیم فاصله را زیاد میکند).
زاویه و محل کویل را ثابت نگه دارید؛ تغییر زاویه عملاً فاصله مؤثر را تغییر میدهد.
از نشانگذاری دقیق روی کلاه/پوست و ثبت %MSO استفاده کنید تا بین جلسات نوسان دوز کم شود.
انتخاب کویل: اگر فوکوس قشری دقیق میخواهید (مثل M1/LDLPFC)، شکلِ هشت ارجح است؛ برای نفوذ کمی عمیقتر (مثل مدیال یا SMA)، دابلکون یا H-coil میتواند کمک کند اما با پذیرش کاهشِ فوکوس.
جمعبندی: هر ۱–۲ سانتیمتر افزایش فاصله، شدت میدان القایی بهطور چشمگیری کم میشود؛ بنابراین TMS اساساً درمانی با نفوذ محدود و قشری است و دوزینگِ دقیق وابسته به فاصله و زاویه کویل، کلید اثربخشی پایدار است.
Double-cone coil
ساختار: دو حلقهی بزرگ که با زاویه نسبت به هم قرار میگیرند تا خطوط میدان در عمق متمرکزتر شوند.
ویژگی فیزیکی: نسبت به شکل-۸ عمق کمی بیشتر میدهد ولی فوکالیتیاش کمتر است؛ برای رسیدن به عمق معمولاً به شدتهای بالاتر نیاز دارد، پس احساس ناراحتی پوستی/عضلانی میتواند بیشتر باشد.
هدفهای رایج: نواحی دور از سطح قشر مانند ناحیه حرکتی پا (leg M1)، SMA و برخی پروتکلهای مخچه (با احتیاط و تنظیمات ایمنی).
مزایا/ملاحظات بالینی: نصب روی بازوی استاندارد دستگاههای rTMS، مناسب برای MEP گرفتن از عضلات اندام تحتانی؛ اما صدای بلندتر و تحریک سطحی قویتر.
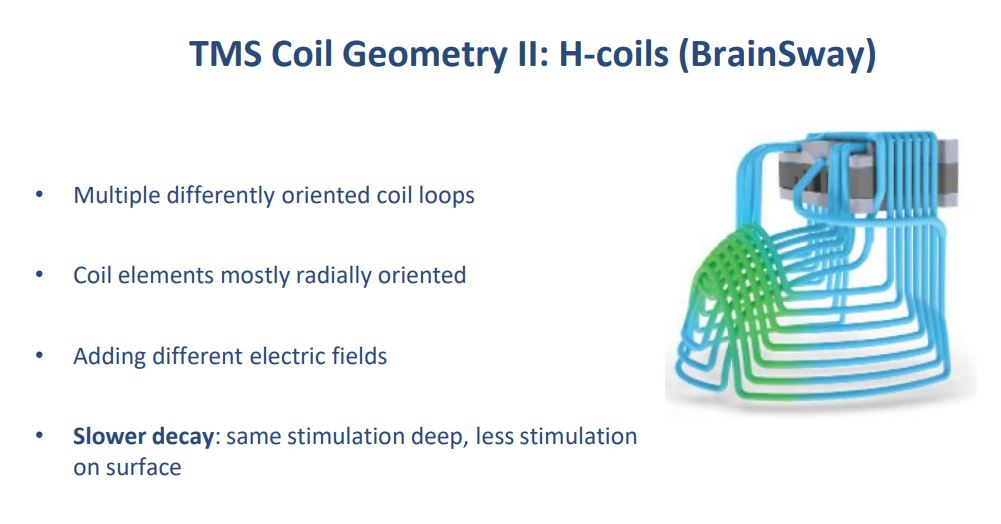
H-coil (BrainSway)
ساختار: مجموعهای از لوپها با جهتگیریهای متفاوت؛ بیشتر عناصر بهصورت شعاعی پیرامون سر چیده شدهاند تا میدانهای الکتریکیِ متفاوت روی هم جمع شوند.
ویژگی فیزیکی: افتِ کندتر میدان با عمق (slower decay) ⇒ برای رسیدن به شدت تحریک یکسان در نواحی عمیق، فشار سطحی کمتری لازم است.
عمق/فوکالیتی: نفوذ عمیقتر اما کمتر فوکال از شکل-۸؛ حجم بافت بزرگتری را پوشش میدهد.
هدفهای رایج: شبکههای میانی/عمیق مانند mPFC / dACC / SMA؛ در درمان افسردگی (H1)، وسواس اجباری OCD (H7) و وابستگی به نیکوتین (H4) تأییدیه/شواهد قوی دارد.
مزایا/ملاحظات بالینی: تحملپذیری بهتر در عمق، اما نیاز به کالیبراسیون اختصاصی MT با همان کلاهکویل؛ هزینه تجهیزات بالاتر و فوکالیتی کمتر.
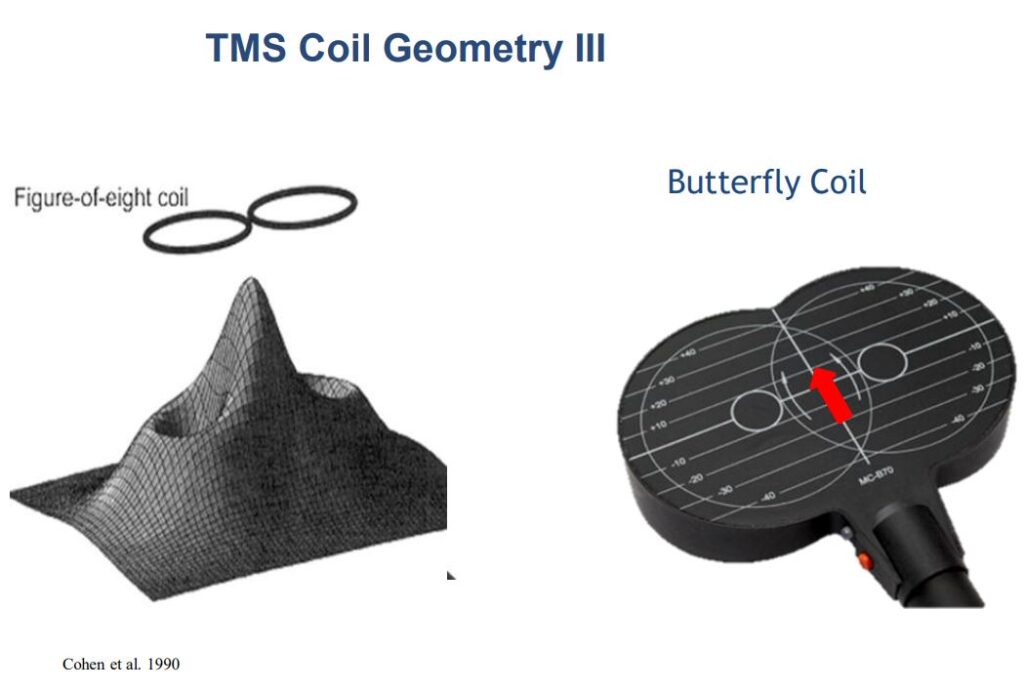
هندسهٔ کویل «پروانهای» (Figure-of-eight / Butterfly)
این کویل از دو حلقهی همجوار تشکیل شده که جریان در آنها در جهتهای مخالف میگذرد. همپوشانی میدانهای مغناطیسیِ دو حلقه باعث میشود بیشترین میدان الکتریکی القایی درست در محل اتصال دو حلقه (فلش قرمز) ایجاد شود.
نتیجهاش تحریک بسیار فوکال است: ناحیهٔ برانگیخته کوچکتر از سایر کویلهاست (استانداردِ نقشهبرداری حرکتی و تنظیم MT).
عمق نفوذ معمولاً کمعمقتر از H-coil و Double-cone است (حدود 1.5 تا 2 سانتیمتر مؤثر)، بنابراین برای اهداف قشری سطحی (مثل M1 یا DLPFC) ایدهآل است.
چرا جهتگیری مهم است؟
میدان مؤثر زمانی بیشینه میشود که مؤلفهٔ مماس با قشر (tangential) بیشترین مقدار را داشته باشد. در ناحیهٔ حرکتی، چرخاندن کویل حدود ۴۵° نسبت به خط میانی معمولاً جریان Posterior→Anterior ایجاد میکند و آستانهٔ حرکتی را کاهش میدهد.
در DLPFC هم ثابتنگهداشتن زاویه و نقطهٔ داغ (hotspot) برای تکرارپذیری حیاتی است.
نکات عملی برای کار بالینی
نقطهٔ داغ دقیقاً بین دو حلقه است؛ همانجا باید روی هدف قرار بگیرد.
فاصلهٔ کویل تا پوست را کم نگه دارید؛ هر میلیمتر فاصله، شدت میدان را کم میکند.
جهتگیری را در شِمای روی کویل علامت بزنید تا بین جلسات یکدست بماند.
برای آستانهگیری (MT) و هدایت دقیق، همین کویل پروانهای انتخاب استاندارد است؛ برای اهداف عمیقتر سراغ Double-cone یا H-coil بروید.
جمعبندی: کویل Figure-of-eight «فوکالترین» گزینهٔ TMS است—بهترین انتخاب برای نقشهبرداری و اهداف قشری سطحی (M1/DLPFC). عمق نفوذ کمتر از کویلهای عمیق است، اما دقت مکانی آن بالاترین است.
4) جهتگیری کویل نسبت به ژیروس (چین ها)
جهت جریان مؤثر، عمود بر «ژیروس» زیر کویل است. به زبان ساده: زاویهٔ کویل نسبت به چینهای قشری مهم است و روی آستانهٔ تحریک و کارایی اثر جدی میگذارد؛ به همین دلیل «زاویهٔ کویل» باید در پروتکل ثبت و ثابت نگه داشته شود.
5) نکات عملی برای کلینیک
پیشفرض قشری: در اغلب دستگاههای استاندارد، محدودهٔ اثر TMS عملاً قشری است؛ برای عمق بیشتر به Double-Cone یا H-coil فکر کنید، اما در ازای کاهش فوکالیتی.
- ثبات زاویه و موقعیت: هنگام نقشهبرداری و جلسات بعدی، زاویهٔ کویل و مکان دقیق را ثابت نگه دارید (پروتکلنویسی و نشانهگذاری روی کلاه/کپ).
- مدیریت شدت و فوکالیتی: بهخاطر داشته باشید که شدت خروجی دستگاه علاوه بر هندسه، روی فوکالیتی اثر دارد؛ شدت بالاتر الزاماً «بهتر» نیست—تعادلِ عمق/کانونیّت را متناسب با هدف بالینی نگه دارید.
فیزیولوژی TMS (روان و کاربردی)
1) TMS دقیقاً چه کاری با نورونها میکند؟
پالس TMS یک میدان الکتریکی گذرا در قشر ایجاد میکند. اگر این میدان بهاندازهٔ کافی قوی باشد، پتانسیل عمل در نورونها راه میافتد؛ یعنی نورون شلیک میکند.
- پس اثر TMS روی همان ارتباطهای الکتروشیمیاییِ نورونها سوار است: شلیکها، انتقالدهندههای عصبی و مدارهای قشری.
2) اثر TMS «وابسته به حالت مغز» است
پاسخ مغز به یک پالس یکسان میتواند در «استراحت» با «فعالیت» متفاوت باشد (state-dependent). همین یک نکته علتِ تفاوتپذیری پاسخها بین افراد/جلسات است و چرا زمانبندی و آمادهسازی بیمار اهمیت دارد.
3) MEP و آستانهٔ حرکتی (MT) — معیار دوزگذاری
وقتی M1 را بزنیم، در عضلهٔ هدف EMG میگیریم: Motor Evoked Potential (MEP). MEP شاخص پایهایِ اثر فوری TMS است.
- Motor Threshold (MT) یعنی حداقل شدت TMS که «یک پاسخ حداقلیِ حرکتی» (مثل توئیچ قابلرؤیت یا دامنهٔ EMG حدود ±0.05 mV) ایجاد کند. MT همان مرجعِ دوزگذاری بهحساب میآید.
- MT «شاخص برانگیختگی قشر» است اما به فاصلهٔ پوستسر تا قشر هم حساس است؛ پس MT را برای هر فرد (و حتی هر نیمکره/ناحیه) جدا کالیبره کنید.
4) تکپالس و جفتپالس: چه چیزهایی میسنجیم؟
با تکپالس (spTMS) میشود MEP، MT، Silent Period و زمانهای هدایت مرکزی را بهدست آورد.
- با جفتپالس (paired-pulse) میتوان مهار/تسهیل درونقشری را بررسی کرد (SICI/ICF)، که پروفایلِ دارویی–گیرندهای متفاوتی دارد (مثلاً مسیرهای GABAergic).
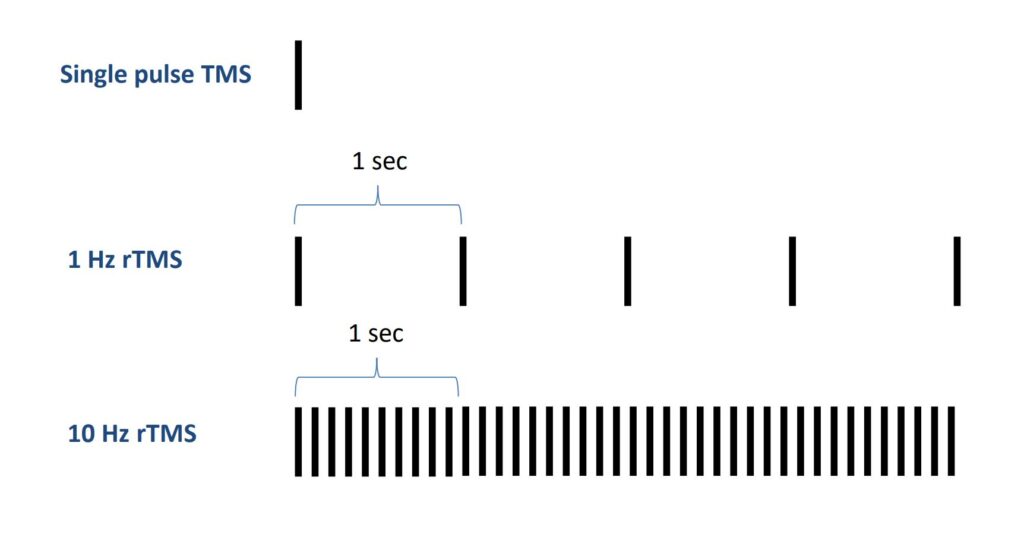
این شکل تفاوت «ریتم تحریک» در TMS را نشان میدهد:
Single-pulse TMS (بالا): هر بار فقط یک پالس زده میشود. بیشتر برای اندازهگیریها و تعیین آستانه حرکتی (MT)، نقشهبرداری قشری و MEP استفاده میشود.
rTMS با فرکانس پایین 1 Hz (وسط): در هر ثانیه یک پالس میآید (فاصلههای خالی بین میلهها همین ۱ ثانیه است). وقتی چند دقیقه ادامه یابد معمولاً باعث کاهش برانگیختگی قشر (LTD-like) میشود. کاربرد رایج: مهار نیمکره راست DLPFC در افسردگی یا مهار نواحی بیشفعال. شدت معمول: حدود 90–100% MT.
rTMS با فرکانس بالا 10 Hz (پایین): در هر ثانیه ده پالس میآید؛ به صورت ترینهای کوتاه با فواصل استراحت انجام میشود (برای ایمنی). این الگو معمولاً باعث افزایش برانگیختگی قشر (LTP-like) میشود. کاربرد رایج: تحریک DLPFC چپ در افسردگی. شدت معمول: 110–120% MT (طبق گایدلاین، با محدودیت طول ترین و فاصله بینترین جهت پیشگیری از تشنج).
خلاصه دیداری: هر میله یک پالس است؛ هرچه میلهها فشردهتر باشند، فرکانس بالاتر است (اثر تحریکیتر). فاصلههای بیشتر = فرکانس پایینتر (اثر مهاریتر).
5) از «پالس» تا «پلاستیسیته»: rTMS چهطور دوام اثر میدهد؟
rTMS بهجای یک شلیک، الگوهای تکراری میزند و مکانیزمهای نوراپلاستیسیته را وارد بازی میکند (اصل «با هم شلیک کن، با هم سیمکشی شو»). نتیجه: LTP/LTD و تغییرات پایدارتری در شبکهها.
قاعدهٔ عملی مشهور:
Low-frequency ≤1 Hz → گرایش به LTD/مهاری،
High-frequency ≥5 Hz → گرایش به LTP/تحریکی.
6) تتابِرست (TBS): iTBS و cTBS به زبان ساده
TBS پالسها را در Burstهای ۳ تایی با 50 Hz میدهد که در ریتم 5 Hz تکرار میشوند؛ پروتکل کلاسیک ۶۰۰ پالس با ۸۰٪ MT است.
- TBS = سه کلیک خیلی سریع (50Hz) که هر ۰٫۲ ثانیه تکرار میشود (5Hz)، تا در مجموع ۶۰۰ کلیک با شدتی نزدیک به ۸۰٪ آستانهٔ شخصی شما اجرا شود؛ حدود ۴۰ ثانیه (cTBS) یا ~۳ دقیقه (iTBS).
- iTBS (intermittent) معمولاً اثر تحریکی شبیه هایفریکوئنسی دارد (پروتکل ~۱۹۰ ثانیه). cTBS (continuous) اثر مهاری شبیه لو-فریکوئنسی میگذارد (~۴۰ ثانیه).
7) «پرایمینگ» و متاپلاستیسیته: چرا همیشه نتیجه یکسان نیست؟
چون اثر TMS به حالت مغز وابسته است، میشود با «پرایمینگ» (مثلاً تحریک قبلی) حالت شبکه را عوض کرد و پاسخ را جهت داد؛ این همان metaplasticity است. در عین حال، هومئوستاز پلاستیسیتی میتواند بخشی از این اثرات را خنثی کند؛ لذا ترتیب/فاصلهٔ پروتکلها مهم است.
نکات بالینی سریع (ترجمهٔ فیزیولوژی به اجرا)
دوزگذاری شخصیسازیشده: همیشه شدتها را برحسب ٪MT فرد گزارش و اعمال کنید؛ تغییر کلاه/کویل یا وضعیت سر میتواند MT مؤثر را عوض کند.
- انتظار تغییرپذیری داشته باشید: بهخاطر state-dependence، کیفیت خواب، دارو، کافئین، اضطراب و حتی زمان روز میتوانند پاسخ را تغییر دهند—پروتکل و جلسه را تا حد ممکن ثابت نگه دارید.
- برای اهداف زمانحساس: اگر درمان افسردگی با زمان روزانهٔ کوتاهتر میخواهید، iTBS گزینهٔ عملیتری نسبت به 10Hz طولانی است (در عین توجه به اندیکاسیون/تحمل بیمار).
«TMS دقیقاً چه میکند؟» (ساده و کاربردی)
سه کار اصلی TMS
Stimulation (تحریک/فعالسازی):
با یک پالس، نورونهای ناحیهٔ هدف را «بهکار میاندازیم». نمونهٔ کلاسیکش روی قشر حرکتی است که با تکپالس، پاسخ عضلانی (MEP) میگیریم؛ این برای پیمایش و تعیین آستانهٔ حرکتی (MT) عالی است.- Disruption (ایجاد اختلال کوتاهمدت/Virtual Lesion):
با پالسهایی در حین اجرای یک تکلیف (آنلاین)، میتوانیم عملکرد یک ناحیه را برای چند صد میلیثانیه مختل کنیم و بفهمیم آن ناحیه در انجام آن کار نقش دارد یا نه. به این میگویند «آسیب مجازی». - Modulation (تعدیل پایدار):
وقتی پالسها را تکراری (rTMS/TBS) میزنیم، ورودیهای قشری طوری «شرطی» میشوند که اثرشان پس از پایان جلسه هم بماند (آثار آفلاین). بسته به الگو، میتواند تحریکی (LTP-like) یا مهاری (LTD-like) باشد.
«آنلاین» در برابر «آفلاین»
آنلاین (Online): اثر فوری TMS حین کار—برای تحریک یا اختلال کوتاهمدت. مثال: وارد کردن پالسها دقیقاً موقعِ تصمیمگیری تا ببینیم عملکرد کند میشود یا نه.
- آفلاین (Offline): اثر پس از پایان پروتکل—ویژهٔ rTMS یا TBS؛ یعنی بعد از 10Hz/1Hz یا iTBS/cTBS، تغییر کارکرد شبکه برای دقایق تا ساعتها باقی میماند.
تکپالس بهعنوان ابزار پیشبالینیِ دقیق
با Single-Pulse TMS علاوه بر پیمایش حرکتی، میتوان شاخصهای فیزیولوژیک زیادی را سنجید: MEP، MT، مهار/تسهیل درونقشری (SICI/ICF)، Silent Period، زمان هدایت مرکزی، تعامل بیننیمکرهای و… (در کنار پروفایلهای دارویی متفاوت). اینها برای پژوهش و تنظیم دوز بالینی پشتوانه میدهند.
از «پالس» تا «پلاستیسیته»
rTMS سازوکارهای پلاستیسیته را درگیر میکند:
Low-frequency ≤1Hz → گرایش به مهاری/LTD-like،
High-frequency ≥5Hz → گرایش به تحریکی/LTP-like.
چه زمانی از هرکدام استفاده کنیم؟
Stimulation (تحریک): نقشهبرداری حرکتی، تعیین MT، سنجش سالمبودن مسیرهای قشری–نخاعی.
- Disruption (اختلال لحظهای): مطالعات نقشسنجی نواحی (زبان، توجه، بینایی، تصمیمگیری) با پالسگذاری زمانمند در میلیثانیههای حساس.
- Modulation (تعدیل پایدار): درمانهای بالینی و نوروهَب—مثلاً افزایش فعالیت DLPFC چپ در افسردگی (10Hz/iTBS)، یا کاهش بیشفعالی شبکه با پروتکلهای مهاری.
ایمنی و دوزینگ در عمل (rTMS/TBS)
1) پیش از شروع هر پالس: اسکرینینگ و رضایت
رضایت آگاهانه: بیمار دقیقاً بداند دورهی TMS شامل چه چیزهایی است؛ بروشور/ویدئو بدهید و در صورت امکان یکی از اعضای خانواده هم در جلسه توضیح حضور داشته باشد.
- اسکرینینگ ایمنی (نمونه پرسشها): سابقهی تشنج/صرع، سنکوپ، ضربهی سر با بیهوشی، و… را پرسوجو کنید.
- ایمپلنتها/فلزات: ایمپلنتهای تحریکگر/ثبتگر (DBS، الکترودهای قشری) میتوانند با میدان TMS جریان القایی بگیرند؛ خطر بالقوه دارند. کویل حداقل ۱۰ سانتیمتر از الکترود/ایمپلنت فاصله داشته باشد. کاشت حلزون گوش، کنترااندیکاسیون مطلق است. ایمپلنتهای «MRI-safe» احتمالاً «TMS-safe» هم هستند، اما با احتیاط.
- بارداری و اطفال: دادههای موجود نشان میدهد TMS در بارداری قابلقبول و ایمن گزارش شده (با ملاحظات وضعیتی مثل شیب لگنی ۳۰° بعد از هفته ۲۴)، و در کودکان/نوجوانان نیز عوارض مشابه بزرگسالان است؛ با این حال طبق دستورالعمل سازنده و قوانین محلی عمل کنید.
- داروها و ریسک تشنج: برخی داروها/مواد آستانه تشنج را پایین میآورند (مثلاً بعضی ضدافسردگیهای سهحلقهای، کلوزاپین، آمفتامینها، کوکائین، الکل…)، قطع برخی داروها (الکل/باربیتورات/بنزودیازپین) نیز خطر دارد؛ در این موارد با احتیاط بیشتر کار کنید.
عوارض شایع و اقدامات کاهش ریسک
سردرد/درد پوست سر: شایع ولی معمولاً خفیف؛ مسکن ساده کفایت میکند.
- شنوایی: صدای کلیک کویل میتواند تا >140 dB باشد؛ حتماً محافظ شنوایی (گوشگیر/ایرپلاگ) بدهید. کاشت حلزون = ممنوع.
- سنکوپ: عمدتاً ناشی از اضطراب/ناراحتی جسمی-روانی؛ پرسنل آماده باشند.
- تشنج: نادرترین ولی جدیترین عارضهی حاد؛ بروز تصادفی بسیار نادر (کمتر از 0.003%). پلن اورژانس داشته باشید؛ >5 دقیقه = اورژانس پزشکی.
3) چارچوب کلی دوزینگ (بدون بازی با پارامترها!)
پارامترها (شدت، فرکانس، طولترِین، فاصلهی بینترِینها) فضای پیچیدهای دارند؛ «با این پارامترها بازی نکنید.» اگر از موجفرمها/ژنراتورهای جدید استفاده میکنید، پایش تشنج الزامی است.
الف) تعیین آستانه حرکتی (MT) و شدت
MT (Motor Threshold) شاخص پایهی شدت تحریک است و توسط پزشک تعیین میشود؛ تعیین MT و محل هدفگیری بهعهدهی پزشک مسئول درمان است.
- در عمل، شدت درمان بهصورت ٪ی از MT تنظیم میشود (مثلاً در پروتکلهای مرسوم rTMS بر اساس RMT و در TBS طبق MTِ تعریفشده در پروتکل). شدت نامناسب = افزایش خطر عارضه/کاهش اثربخشی.
ب) پروتکلهای درمانی رایج (Depression مثال)
rTMS مرسوم: «فرکانسبالا روی قشر پیشپیشانی چپ (DLPFC)، ۵ روز در هفته، به مدت ۴–۶ هفته» بهعنوان استاندارد بالینی طرح درمان ذکر شده است؛ جلسات نگهدارنده بنا به نیاز.
TBS (تتابرست):
الگوی پالس: قطارهای ۳ پالس با 50 Hz که با ریتم 5 Hz تکرار میشوند (الگوی iTBS/cTBS).
- دُز کلاسیک: ۶۰۰ پالس در هر جلسه (iTBS یا cTBS).
- شدت: برای iTBS شدت %120 RMT . الزاماً به دستورالعمل دستگاه/پروتکل مرکز خودتان پایبند باشید.
- ایمنی TBS: مطالعات مرجع نشان میدهد TBS بهطور کلی ایمن است؛ نرخ عوارض مشابه بزرگسالان در اطفال گزارش شده.
نکتهی عملی: اگر TBS را اجرا میکنید، به تکمیل پالس (۶۰۰) و شدت صحیح نسبت به MT خیلی دقت کنید؛ تغییرات ناخواسته (کاهش بیشازحد شدت/پالس) معمولاً اثرگذاری را کم و تغییرات بیرویه (افزایش شدت/تعداد) ریسک را بالا میبرد.
رویهها و نقشها در کلینیک
SOPهای رسمی (دستورالعمل عملیاتی استاندارد) برای آموزش، حفظ مهارت، و مستندسازی رعایت فرآیندها داشته باشید.
- پزشک مسئول: مدیریت روزانهی طرح درمان، تعیین MT/شدت، و لوکالیزهکردن ناحیهی هدف.
- پلن اورژانس تشنج و آگاهی تیم از اقدامات (تماس اورژانس، عدم مهار فیزیکی خشن، تشنج >۵ دقیقه = اورژانس).
هدفگیری و لوکالیزیشن (کجا و چگونه کویل را بگذاریم؟)
چرا لوکالیزیشن اینقدر مهم است؟
اثر درمان وابسته به این است که میدان القایی دقیقاً به شبکهٔ درست برسد.
تکرارپذیری جلسات (روزانه/هفتگی) بدون نشانهگذاری دقیق تقریباً غیرممکن است.
ایمنی و دوزگذاری هم به موقعیت و زاویهٔ کویل وابسته است (بهویژه نسبت به چینهای قشری/ژیروس).
روشهای رایج لوکالیزیشن DLPFC (افسردگی)
هدف کلاسیک: قشر پیشپیشانی پشتی–جانبی چپ (Left DLPFC)
1) «۵ سانتیمتری» (قدیمی و کمدقت)
از نقطهٔ حرکتی (Hotspot) شست، ۵ سانتیمتر قدامی میرویم.
مزیت: سریع و بدون ابزار.
ضعف: خطای زیاد بهخاطر تفاوت اندازهٔ سر و آناتومی افراد.
توصیه: فقط اگر هیچ ابزار دیگری ندارید و برای کار پژوهشی/بالینی مدرن، مناسب نیست.
2) روش Beam F3 (عملاً استانداردِ بدون MRI)
از اندازهگیریهای سیستم 10–20 (دور سر، فاصله ناسـیون–اینیون، فاصله تراگوسها…) استفاده میکند تا نقطهٔ F3 را دقیق روی پوست سر مشخص کند (نزدیکترین تخمین غیرتصویری برای DLPFC).
ابزار کار شما: متر انعطافپذیر + ماژیک پوست + (در صورت امکان) کلاه/کپ 10–20.
کاربردی:
Cz را دقیق علامت بزنید (میانهٔ ناسـیون–اینیون و میانهٔ دو تراگوس).
با محاسبات 10–20 (یا Beam F3 Calculator) نقطهٔ F3 را روی نیمکرهٔ چپ مشخص کنید.
مارک دائمی جلسه: روی کلاه/سر علامت کوچک بزنید و عکس استاندارد بگیرید (از بالا، نیمرخ، روبهرو).
مزیت: دقت خوب، تجهیزات ساده.
ضعف: اندکی زمانبر در جلسهٔ اول؛ به دقت اندازهگیری حساس است.
3) نوروناویگیشن مبتنی بر MRI (دقیقترین)
MRI ساختاری فرد + سیستم دوربین/مارکر → تصویر زندهٔ موقعیت کویل نسبت به هدف.
مزایا: بیشترین دقت، تکرارپذیری عالی، قابلیت اصلاح زاویه/عمق، تصحیح فاصله پوست–قشر.
معایب: هزینه و نیاز به تجهیزات/آموزش.
اگر نوروناویگیشن دارید، حتماً عکس و گزارش مختصات هدف (مثلاً در مختصات MNI یا تصویری) را در پروندهٔ بیمار ذخیره کنید.
زاویهٔ کویل و جهت E-Field
روی DLPFC چپ، معمولاً دستهٔ کویل به سمت خلف–جانبی و صفحهٔ کویل با زاویهٔ ~۴۵° نسبت به شیار ساجیتال قرار میگیرد تا جریان مؤثر عمود بر ژیروس جاری شود.
ثابت نگه داشتن زاویه بهاندازهٔ خودِ نقطه اهمیت دارد؛ در هر جلسه همان زاویه را تکرار کنید (با رفرنس عکس/کلاه/گاید).
عمق و فاصلهٔ پوست–قشر (SCD)
هرچه فاصلهٔ پوست تا قشر در ناحیهٔ هدف بیشتر باشد، برای رسیدن به میدان مؤثر باید شدت بیشتر بدهید.
اگر نوروناویگیشن دارید، از Depth Correction نرمافزار استفاده کنید.
اگر ندارید، حداقل SCD ناحیه هدف را روی کلاه/سر اندازه بگیرید و در برگه درمان ثبت کنید تا در جلسات بعدی مرجع ثابتی داشته باشید. (از تغییرات ناگهانی شدت بدون توجیهِ فنی/بالینی خودداری کنید.)
چکلیست «جلسهٔ اول» (لوکالیزیشن و مستندسازی)
Hotspot حرکتی (M1) را بیابید و MT را تعیین کنید.
یکی از روشهای لوکالیزیشن DLPFC را انتخاب و نقطهٔ هدف را مارک کنید (Beam F3/نوروناویگیشن).
زاویهٔ کویل را مشخص و یادداشت کنید. زاویه کویل در تمام جلسات یک فرد باید ثابت باشد. خط جلوی کویل را روی کلاه علامت بزنید تا این زاویه همیشه تقریبا ثابت باشد (مثلاً «۴۵° Posterior–Lateral handle»).
سه عکس استاندارد بگیرید (Top/Side/Front) و در پرونده ذخیره کنید.
SCD (فاصله پوست–قشر یا معادل عملی) را ثبت کنید.
شدت پایهٔ درمان (بهصورت ٪ از MT) + پروتکل انتخابی + تاریخ/ساعت را بنویسید.
نگهداری تکرارپذیری در جلسات بعدی
از همان کلاه/نقطه/زاویه/ارتفاع صندلی/تکیهگاه استفاده کنید.
هر جلسه قبل از شروع قطارها، ۲۰–۳۰ ثانیه وقت بگذارید و با نگاه به عکسها «کپی دقیق» بسازید.
اگر بیمار تغییر قابل توجه در وزن، مدل مو، درد پوست سر یا وضعیت گردنی دارد، یادداشت کنید؛ گاهی نیاز به ±۵٪ اصلاح شدت دارید (طبق پروتکل مرکز و تحمل بیمار).
هدفگیری در اندیکاسیونهای دیگر (خیلی خلاصه)
OCD: معمولاً پروتکلهای عمقی/شبکهٔ فرونتو–مدیال/سینگولیت قدامی با کویلهای خاص (مثلاً خانوادهٔ H).
درد نوروپاتیک/پس از سکته: M1 قرینهٔ ناحیهٔ درد/گرفتاری (High-Frequency یا iTBS بسته به پروتکل).
وزن/اعتیاد/وسوسه: هدفهای فرونتال–اینسولار/شبکهٔ کنترل شناختی در پروتکلهای خاص پژوهشی–بالینی.
نکته: حتماً مطابق راهنماهای کشور/سازنده و پروتکلهای تاییدشدهٔ مرکز عمل کنید.
اشتباهات متداول و راهحل
جابهجایی روزانهٔ نقطه → راهحل: مارک دقیق + عکس سهنما + استفاده از کپ 10–20.
زاویهٔ متغیر → راهحل: روی کلاه زاویه را هم مشخص کنید.
شدت ثابت بدون توجه به SCD → راهحل: SCD را یکبار ثبت و در صورت تغییر محسوس شرایط بیمار، بهطور مستند اصلاح جزئی انجام دهید.
درد پوست سر/تحمل پایین → راهحل: جابجایی میلیمتری نقطه روی پوست، Pre-Med مسکن ساده، شروع با Warm-up چند قطار کوتاه.
انتخاب پروتکل بر پایهٔ تشخیص (Clinical Indication → Target & Protocol)
در این بخش، رایجترین تشخیصها، ناحیهٔ هدف، و پارامترهای عملیاتی را بهصورت «قابل اجرا در کلینیک» بر اساس مطالعات موجود خلاصه کردهایم.
1) اختلال افسردگی اساسی (MDD)
هدف استاندارد: DLPFC چپ (نقطهٔ F3 با Beam/F3 یا نوروناویگیشن)
گزینههای پروتکل:
10Hz روی DLPFC چپ: ~۴ ثانیه ON / ۱۱ ثانیه OFF، حدود ۳۰۰۰ پالس در هر جلسه، شدت ≈ ۱۲۰٪ rMT، معمولاً ۵ جلسه/هفته برای چند هفته (دورهٔ کامل ۲۰–۳۰ جلسه).
- iTBS روی DLPFC چپ: ۶۰۰ پالس در ≈۳ دقیقه، در مطالعات «غیرکمتر از 10Hz» گزارش شده و برای کلینیکهای پرمراجعه بسیار زمانکارآمد است. شدت معمولاً حوالی ۱۲۰٪ rMT ( iTBS/10Hz از نظر اثربخشی نزدیک گزارش شدهاند).
- ۱Hz روی DLPFC راست: گزینهٔ کمریسکتر از نظر تحریکپذیری شبکه، با شواهد مفید بودن در افسردگی؛ شدت معمولاً ۱۰۰–۱۱۰٪ rMT و دورهٔ چند هفتهای.
- دوطرفه (Right 1Hz → Left 10Hz): ابتدا مهاری راست سپس تحریکی چپ؛ برای موارد مقاوم و فنوتیپهای با ناهمگونی شبکهٔ پیشپیشانی.
نکات تصمیمگیری:
اگر زمانِ یونیت محدود است یا بیمار «تحمل زمانی» پایینی دارد، iTBS انتخاب عالی است.
- در بیماران مقاوم، تمدید دوره تا ۳۰+ جلسه یا استفاده از دوطرفه منطقی است. دادههای دنیای واقعی نرخ پاسخ/رمیسیون قابلقبولی را نشان میدهند.
2) اختلال وسواس فکری-عملی (OCD)
هدف: mPFC/ACC (پیشپیشانی میانی/سینگولیت قدامی) — غالباً با Deep TMS (H7) و Symptom Provocation کوتاه قبل از پالسدهی برای درگیر کردن مدار.
رویکرد: پروتکلهای H-coil با جلسات روزانه طی چند هفته، همراه تحریک مناطق عمقی مدار وسواس. (هدفگیری mPFC/ACC و استفاده از پروووکیشن.)
Symptom Provocation یعنی چی؟
بهزبان ساده: قبل از شروع تحریک عمیق OCD (مثلاً با H-coil روی mPFC/ACC)، ما عمداً نشانهها/فکرها/موقعیتهایی را که وسواس و اضطراب بیمار را فعال میکند، خیلی کوتاه و کنترلشده یادآوری میکنیم تا مدارهای مرتبط با وسواس «روشن» شوند. بعد، TMS را دقیقاً روی همین مدارِ فعال میزنیم تا اثر تعدیلی (Modulation) بیشتری بگیریم. به این روشنکردن عمدیِ علائم، Symptom Provocation میگویند.
چرا انجامش میدهیم؟
پاسخ TMS وابسته به حالت مغز است. وقتی مدارِ وسواس فعال باشد، تحریک هدفمندتر و پلاستیسیتی کارآمدتر میشود.
در پروتکلهای OCD (بهویژه Deep TMS)، این کار با شواهد بالینی همراه است که نتیجه درمان را بهتر میکند.
چطور عملی انجام میدهیم؟ (الگوی ۵ مرحلهای کوتاه)
انتخاب محرکها: بر اساس «وسواسِ غالب» بیمار (آلودگی، وارسی، تقارن، افکار مزاحم…) یک فهرستِ ۳–۵ موردی از سرنخهای سریع آماده کن (تصویر، کلمه، شیء، سناریوی ۱۰–۲۰ ثانیهای).
ارزیابی شدت پایه: از بیمار SUDS بگیر (شدت ناراحتی ۰ تا ۱۰).
برانگیزش کوتاه (۲–۵ دقیقه): محرکها را یکییکی ارائه بده تا SUDS به حدود ۴–۶ از ۱۰ برسد (کافیست «متوسط» شود؛ قرار نیست طوفان اضطراب درست کنیم).
شروع تحریک: بلافاصله TMS را آغاز کن. اگر پروتکل اجازه میدهد، نشانههای حداقلی را بین ترنها حفظ کن تا مدار فعال بماند.
پایان و جمعبندی: چند دقیقه دیاسترس (آرامسازی/تنفس)، سپس SUDS نهایی و یادداشتبرداری.
مثالهای محرک برانگیز
آلودگی/شُستوشو: دستکش آلودهٔ تمثیلی، تصویر دستگیرهٔ درِ عمومی، گفتنِ «فرض کن الان…».
وارسی: سناریوی «اجاق گاز/قفل در»، عکس قفل نیمهباز.
افکار مزاحم: خواندن چند جملهٔ کوتاه «Trigger» که قبلاً با درمانگر نوشتهاید.
نکات ایمنی و اخلاقی
رضایت آگاهانه + کلمهٔ امن برای توقف.
هدف برانگیزش متوسط و کنترلشده است؛ نه غرقهسازی شدید.
در بحرانهای فعال (خطر خودآسیبی، پانیک کنترلنشده)، اول مدیریت بالینی سپس TMS.
مستندسازی: محرک استفادهشده، SUDS پیش/پس، تحمل بیمار.
3) درد نوروپاتیک و فیبرومیالژی
هدف اصلی: M1 کنترالترال با ناحیهٔ درد (یا دوطرفه در برخی فنوتیپها)
پروتکل نمونهٔ M1 (حرکتی):
۱۰Hz، حدود ۲۰۰۰ پالس/جلسه، ۸۰–۹۰٪ rMT، ۱۰+ جلسه (۵ جلسه/هفته). شواهد «A: قطعاً مؤثر» برای درد نوروپاتیک و «B: احتمالاً مؤثر» برای فیبرومیالژی گزارش شده است.
نکتهٔ اجرایی: در دردهای یکطرفه، طرف مقابلِ درد را روی M1 هدف بگیرید؛ در فیبرومیالژیِ منتشر میتوان به رویکردهای گستردهتر و تعداد جلسهٔ بیشتر فکر کرد.
4) وزوز گوش (Tinnitus)
هدف: قشر شنوایی (بین T3–T5 برای سمت چپ؛ بسته به لاترالیتی)
پروتکل با شواهد کلاسیک:
۱Hz مداوم بهمدت ۲۵ دقیقه (~۱۵۰۰ پالس)، ۱۱۰٪ rMT، ۵ روز/هفته برای ≥۲ هفته. سطح شواهد C (اثر «امیدبخش اما نامعنا» در متاآنالیزهای قدیمیتر؛ ناهمگنی بالاست).
5) PTSD (اختلال استرس پس از سانحه)
رویکردها: شواهد در حال رشد؛ پروتکلهای ۱Hz روی DLPFC راست یا HF/iTBS روی چپ بررسی شدهاند، اما ناهمگنی در پارامترها زیاد است و نیاز به شخصیسازی دارد (همراهی با درمانهای مبتنی بر مواجهه و رواندرمانی میتواند سودمند باشد).
جمعبندی عملی برای کلینیک
افسردگی: از 10Hz چپ یا iTBS چپ شروع کنید؛ در مقاومها دوطرفه را در نظر بگیرید.
- OCD: Deep TMS (H7) با هدف mPFC/ACC و Provocation پیش از تحریک.
- درد نوروپاتیک/فیبرومیالژی: M1 با 10Hz، ۲۰۰۰ پالس، ۸۰–۹۰٪ rMT، ۱۰+ جلسه.
- وزوز گوش: ۱Hz بر قشر شنوایی (T3–T5)، ۱۵۰۰ پالس، ۵×/هفته × ≥۲ هفته (سطح C).
- PTSD: پروتکلها متنوع؛ انتخاب هدف/فرکانس را با فنوتیپ علائمی و همدرمانیها همسو کنید.
فلوچارت عملی دورهٔ درمان (از پذیرش تا پایان و نگهدارنده)
این بخش، یک الگوی «قابل اجرا در کلینیک» بر اساس مقالات موجود میدهد تا تیم اتاق TMS—از پذیرش تا ثبت نتیجه—همهچیز را استاندارد و تکرارپذیر پیش ببرند.
۱) پیش از شروع دوره (Intake & Baseline)
آموزش + رضایت آگاهانه
پیش از هر چیز، یک توضیح دقیق و شفاف به بیمار و در صورت امکان خانواده بدهید (چی هست، چند جلسه، عوارض شایع، نرخ موفقیت، جایگزینها) و سپس رضایت کتبی بگیرید.
غربالگری ایمنی (چکلیست کوتاه)
سابقهٔ تشنج/سنکوپ/ضربهٔ سر، مشکلات شنوایی/تینیتوس، کاشتهای حلزونی/قلبی و سایر ایمپلنتها، بارداری، فلزات داخل جمجمه، پمپ دارویی، داروهای جاری، تجربهٔ قبلی TMS/MRI و مشکلات احتمالی. همین چند سؤال ساده، ریسک را بهخوبی مشخص میکند.
اسکیلهای پایه (Baseline Outcomes)
برای افسردگی، اسکیلهای PHQ-9 / IDS-SR / BDI را بهصورت استاندارد ثبت کنید تا «سود بالینی» به شکل عینی قابل رصد باشد. (حداقل یکی از اینها الزامی باشد.)
نکتهٔ عملی: متناسب با اندیکاسیون، میتوانید اینها را اضافه کنید:
OCD: OCI-R، اضطراب: GAD-7، PTSD: PCL-5، درد: VAS/NRS، وزوز: THI، برداشت کلی پزشک/بیمار: CGI-S/I. (هفتگی یا دوهفتهیکبار تکرار شوند.)
۲) چیدمان اتاق و «چک قبل از شروع» هر جلسه
ایمنی و پایش
«پایش بالینی مداوم»، آمادهبودن برای مدیریت فوریتها (در صورت بروز تشنج)، و استفاده از محافظ گوش را در SOP بنویسید و تیم را آموزش دهید.
لوکالیزیشن و پارامترها
نقطهٔ هدف، زاویهٔ کویل، شدت (٪ از rMT)، و پروتکل همان جلسهٔ اول باشد (عکس سهنما/مارک روی کپ کمک میکند).
قبل از قطارها: ۳۰–۶۰ ثانیه تطبیق دقیق با عکس/مارکر، و تأیید تحمل بیمار.
۳) برنامهٔ جلسات و دوزگذاری دوره
الگوی استاندارد افسردگی (نمونهٔ مرجع برنامهریزی):
High-Frequency چپ (DLPFC)، پنج جلسه در هفته، ۴–۶ هفته (۲۰–۳۰ جلسه)؛ یا معادل آن با iTBS (زمان کوتاهتر، اثربخشی همتراز در مطالعات).
بدانیم چه چیزی «واقعاً» کار میکند؟
MDD: «قطعاً مؤثر» در مرورهای شواهد.
PTSD: «احتمالاً مؤثر».
درد نوروپاتیک: «قطعاً مؤثر». (فیبرومیالژی: احتمالاً مؤثر).
وزوز: «ممکن است مؤثر» (شواهد ناهمگون).
۴) پلن پایان دوره و نگهدارنده (Post-treatment Planning)
دربارهٔ پایان تدریجی (Fade-out) یا قطع یکباره تصمیم بگیرید؛ برخی مراکز ۱–۲ هفته کاهش دفعات میدهند تا ثبات ایجاد شود.
Follow-up/Boosterها را مشخص کنید (مثلاً بسته به برگشت علائم، چند جلسهٔ تقویتی در ماههای بعد). این موارد را از ابتدا به بیمار توضیح دهید تا انتظار واقعبینانه داشته باشد.
۵) شتابداده (Accelerated TMS) — برای کیسهای منتخب و زمان محدود
الگوی SAINT/SNT: ۱۰ نوبت iTBS در روز (فاصلهٔ حدود ۵۰ دقیقه بین نوبتها)، ۵ روز پشتسرهم؛ در گزارشها، نرخ پاسخ/رِمیشن بسیار بالا گزارش شده است (وابسته به انتخاب کیس، شدت، تناوب، لوکالیزیشن دقیق).
نکتهٔ تخصصی: انتخاب کیس، رعایت فاصلهٔ بین نوبتها، و انطباق دقیق هدفگیری (Beam F3/نوروناویگیشن) در موفقیت شتابداده حیاتی است.
۶) مدیریت کیفیت (SOP) و نقشها
آموزش رسمی (دانشگاهی/شرکتی/Peer-to-Peer) + SOP مکتوب برای آموزش، نگهداشت مهارت، و مستندسازی پایبندی تیم.
نقش پزشک مسئول: تعیین MT و شدت، لوکالیزیشن، مدیریت روزانهٔ پلن درمان.
تنظیم انتظارات بیمار (Course length, احتمال نیاز به نگهدارنده).
۷) رهگیری نتیجه (During-/Post-Course Outcomes)
پروتکل پیشنهادی پایش:
هفتگی: PHQ-9 (یا IDS-SR/BDI—ثابت بمانید تا مقایسهپذیر باشد).
پایان دوره: همان اسکیل پایه + CGI-I؛ یادداشت بالینی از تغییرات خواب/انرژی/کارکرد.
فواصل بعدی (۴–۸ هفته پس از اتمام): پیگیری برای نیاز احتمالی Booster.
همزمانی با دارو/رواندرمانی و مدیریت عوارض حین درمان
در این بخش، دستورعملهای «قابل اجرا در کلینیک» که دقیقاً موقع کار با بیمار به درد بخوره—جایی که باید همزمانی با داروها رو بسنجیم، عوارض شایع رو مدیریت کنیم، و شرایط خاص (سنکوپ، اضطراب، تحمل درد پوستسر…) رو بدون استرس جمع کنیم.
1) همزمانی TMS با داروها (Medication Co-administration)
اصل کلیدی: TMS معمولاً کنار درمانهای دارویی ادامه پیدا میکند؛ اما از منظر ایمنی، بدانید که بعضی داروها آستانهٔ تشنج را پایین میآورند (ضدافسردگیها و نورولپتیکها) و ضدّ تشنجها ریسک را کاهش میدهند. بنابراین، برنامهٔ تحریک را با نسخهٔ بیمار هماهنگ کنید و در تغییرات مهم دارویی، احتیاط را بالا ببرید.
فهرست هشدارها:
خطر بالقوهٔ قوی: ایمیپرامین، دوکسپین، آمفتامینها، کلوزاپین، کوکائین، الکل… → با احتیاط زیاد.
- خطر نسبی: میانسِرین، فلوکستین، هالوپریدول، پنیسیلین، آنتیهیستامینها… → با احتیاط.
- خطر قوی در قطع ناگهانی: الکل، باربیتوراتها، بنزودیازپینها… → با احتیاط (از قطع ناگهانی پرهیز کنید).
آپدیت مهم: با دادههای جدید، نرخ تشنج بهقدری پایین گزارش شده که میزان «احتیاطِ قبلاً توصیهشده» دیگر حمایت قوی ندارد—یعنی رویکرد معقول و استاندارد کافی است، نه اضطراب بیشازحد.
نکتهٔ عملی: اگر دارویی با ریسک تشنج اضافه/حذف شد، همان روز مانیتورینگ دقیقتر و در جلسهٔ بعد ارزیابی تحمل/شدت انجام دهید. هدف، حفظ اثربخشی با حداقل ریسک است.
2) ترکیب با رواندرمانی (Psychotherapy)
در عملِ کلینیکی، همافزایی TMS با CBT/ACT/Exposure رایج است (برای افسردگی، اضطراب، PTSD). توصیهٔ: در جلسات پرتکرار (۵ جلسه در هفته)، هر هفته حداقل یک سِشن کوتاه رواندرمانی ساختارمند یا تمرین خانگی را کنار TMS تنظیم کنید تا انتقال تغییرات عصبی به مهارتهای رفتاری تسهیل شود.
همزمانی با رواندرمانی تداخلی با ایمنی ندارد؛ بیشتر جنبهٔ بهینهسازی نتیجهٔ بالینی و «انتقال به دنیای واقعی» دارد.
3) مدیریت عوارض شایع و سناریوهای داخل اتاق
سردرد/درد پوستسر/ناراحتی
شیوع حدودی: سردرد ~۱۰٪؛ سفتی/درد گردن ~۱٪. مسکنهای ساده معمولاً کافیاند (قبل یا بعد از جلسه). به تنظیم زاویهٔ کویل، فشار تماس، و پد نرم هم توجه کنید.
شنوایی
پالس TMS «صدای ضربه» میسازد که میتونه به شدت بالای ۱۴۰ دسیبل برسد؛ محافظ گوش برای بیمار و اپراتور اجباری باشد. ایمپلنت حلزون گوش: منع مطلق.
سنکوپ (غش vasovagal)
یک واکنش شایع به اضطراب/ناراحتی است: علائم اولیه (سرگیجه، تهوع، عرق سرد) را جدی بگیرید؛ توقف تحریک، درازکش با بالاآوردن پا، آب/قند سبک، تهویهٔ اتاق… سپس با اطمینانبخشی و جلسهٔ کوتاهتر/رامپ ملایمتر ادامه دهید.
تغییرات EEG پس از جلسه
پساثرهای EEG تا ۲۰–۷۰ دقیقه گزارش شدهاند؛ در زمان ترخیص لحاظ کنید (عجله برای رانندگی نداشته باشند).
تشنج (بسیار نادر)
نادرِ نادر: کمتر از ۰٫۰۰۳٪. دو بازهٔ نظری وقوع: حین/بلافاصله بعد از قطارها و در فاز پساثر. یک پلن اورژانسی مکتوب داشته باشید: محیط را ایمن کنید، از مهار فیزیکی شدید پرهیز، اکثر تشنجها خودمحدود میشوند؛ >۵ دقیقه = اورژانس (تماس اورژانس/پزشک).
4) انتخاب و پایش پارامترها (برای ایمنی و تحمل بهتر)
پارامترها (شدت، فرکانس، فاصلهٔ بین قطارها، طول جلسه) را بیحساب تغییر ندهید؛ با پروتکلهای استاندارد شروع کنید، سپس بهصورت تدریجی و مستند تنظیم کنید.
- TBS (iTBS/cTBS) از نظر ایمنی در منابع کلاسیک (Oberman 2011؛ Rossi 2009) پشتیبانی دارد.
- اثر حالت (State-dependent): پاسخ TMS به «وضعیت» سیستم عصبی بستگی دارد (خواب، کافئین، اضطراب، داروها…)، پس ثبات شرایط تا حد ممکن مفید است.
5) جمعیتهای خاص و ایمپلنتها
بارداری: دادههای موجود «نتایج بالینی مثبت و عوارض شدید گزارش نشده» را نشان میدهد؛ از Tilt لگنی ۳۰ درجه از هفتهٔ ۲۴ به بعد برای پیشگیری از افت فشار خوابیده به پشت استفاده شود. همیشه قوانین محلی/راهنمای سازنده را چک کنید.
- کودکان/نوجوانان: درمان شدهاند (افسردگی، ADHD، تورت، میگرن)؛ عوارض مشابه بزرگسالان.
- الکترودهای عمقی/کورتیکال: امکانپذیر اما با احتیاط؛ حداقل ۱۰ سانتیمتر فاصله از لیدها، و توجه به «MRI-safe بودن» ایمپلنت بهعنوان شاخص همخوان با «TMS-safe».
6) پروتکل «آرامتر و قابلتحملتر» برای بیماران حساس
رامپ تدریجی شدت طی چند جلسهٔ اول (مثلاً از ۹۰٪ rMT به ۱۲۰٪ rMT).
پد/کوشن زیر کویل، زاویهٔ بهینه، استاپهای کوتاه بین قطارها.
مسکن ساده ۳۰–۶۰ دقیقه پیش از جلسه در افرادی که سردرد تکرارشونده دارند.
- کاهش اضطراب: توضیح قبل از شروع، گوشگیر مناسب، دموبازدم، و اگر لازم بود جلسهٔ کوتاهترِ آشنایی (familiarization) قبل از ورود به دورهٔ اصلی.
7) چکلیست داخل اتاق (قابل پرینت و چسباندن)
محافظ گوش؟ بله / خیر.
زاویهٔ کویل و نقطهٔ هدف با عکس مرجع مطابقت دارد؟ بله / خیر.
شدت برحسب ٪ rMT، پروتکل، تعداد پالسها ثبت شد؟ بله / خیر.
تحمل بیمار (درد/اضطراب/سرگیجه) چک شد؟ بله / خیر.
علائم سنکوپ/تشنج؟ خیر (در صورت بروز: اجرای پلن).
پاسخ، رمیسیون، بوستر/نگهدارنده و «الگوریتم عدمپاسخ» (کاملاً اجرایی)
این بخش طوری نوشته شده که تیم اتاق TMS بتواند وسط دورهٔ درمان تصمیم دقیق بگیرد، درمانهای موفق را تثبیت کند و در صورت عدمپاسخ مسیر جایگزین روشن داشته باشد.
1) تعاریف استانداردِ نتیجه
Response (پاسخ): کاهش ≥ ۵۰٪ نسبت به نمرهٔ پایه (مثلاً PHQ-9، BDI، IDS-SR).
Remission (رِمیشن/بهبودی کامل): رسیدن به محدودهٔ «طبیعی/خیلی خفیف»
PHQ-9 ≤ 4–5
BDI-II ≤ 9–10
IDS-SR ≤ 14
CGI-I = 1 یا 2 (خیلی بهتر/بسیار بهتر)
MCID (حداقل تغییر بالینی مهم): افت ≥ ۵ امتیاز در PHQ-9 یا افت معنادار در ابزار پایهٔ منتخب شما.
نکتهٔ عملی: از «همان ابزار پایه» برای تمام پایشها استفاده کنید تا نمودار روند قابل تفسیر باشد.
2) ایستگاههای تصمیمگیری در طول دوره
جلسهٔ 10–12: باید سیگنال اولیهٔ بهبود (≥20٪) دیده شود.
جلسهٔ 15–20: در مسیر پاسخ ≥35–40٪ باشید؛ در غیر این صورت آمادهٔ اصلاح پروتکل شوید.
پایان دورهٔ 20–30 جلسه: انتظار پاسخ ≥50٪ و در بخشی از بیماران رمیسیون.
3) اگر تا جلسهٔ 10–12 سیگنال مثبت نداریم؛ اول «پایهها» را چک کنید (10-Point Check)
لوکالیزیشن: نقطهٔ هدف درست است؟ (Beam F3 یا نوروناویگیشن)
زاویهٔ کویل: ~۴۵° نسبت به خط میانی/شیار ساجیتال ثابت مانده؟
شدت واقعی: رفرِش rMT/RMT (نوسان روزانه ±۱۰٪ طبیعی است)؛ شدت فعلی مطابق پروتکل؟
تعداد پالسها: به سقف پروتکل میرسید؟ (مثلاً ۳۰۰۰ پالس برای 10Hz یا ۶۰۰ برای iTBS)
فاصلهٔ پوست–قشر (SCD): تغییر محسوس نکرده؟ (مدل مو/زاویه/کلاه)
تحمل بیمار: درد پوست سر/اضطراب باعث کاهش شدت/پالس نشده؟
همزمانی داروها: تغییرات جدید (افزایش ریسک تشنج/کاهش تحمل)؟
خواب/کافئین/الکل: وضعیت پایدار است؟
شاخصهای پایهٔ اشتباه: آیا نمرهٔ پایه درست مستند شده؟ ابزار ثابت بوده؟
پایبندی: غیبت/وقفهٔ طولانی بین جلسات نداشتید؟
۸۰٪ موارد «عدم سیگنال زودهنگام» با همین چکلیست فنی/رفتاری حل میشود.
4) الگوریتم عدمپاسخ (Non-Response Algorithm)
گام A — بهینهسازی تکنیک
rMT را دوباره بگیرید و شدت را تا ۱۲۰–۱۳۰٪ rMT (طبق دستورِ پروتکل مرکز و تحمل بیمار) پلهای +۵٪ بالا ببرید.
زاویه/فشار کویل را استاندارد کنید (عکس سهنما، گونیومتر ساده).
لوکالیزیشن را بازبینی کنید (Beam F3 دقیقتر، یا اگر دارید نوروناویگیشن).
پالس/جلسه را کامل کنید: 10Hz ≈ ۳۰۰۰ پالس | iTBS = ۶۰۰ پالس.
گام B — تنظیم دوز/جلسات
تمدید دوره تا ۳۰–۳۶ جلسه اگر پاسخ «در حال شکلگیری» است (مثلاً 20–35٪).
دو نوبت در روز (فقط در مراکز آماده و کیسهای انتخابشده) یا الگوهای شتابداده (iTBS با فاصلههای ۴۵–۵۰ دقیقهای) برای مقاومها.
گام C — تغییر پروتکل
از 10Hz چپ → iTBS چپ (یا برعکس) سوئیچ کنید.
دوطرفه را امتحان کنید: 1Hz راست سپس HF/iTBS چپ (بهویژه در اضطراب بالا).
اگر فنوتیپ مناسب دارد، 1Hz راست تکطرفه (افسردگی با تحریکپذیری/اضطراب برجسته).
گام D — ملاحظات بالینی
بیخوابی/درد/اختلال مصرف را درمان همزمان کنید.
رواندرمانی ساختارمند (CBT/ACT/Exposure) را موازی کنید.
در مقاومت شدید/خطر بالا: Deep TMS (هدف mPFC/ACC)، لوکالیزیشن پیشرفته، یا ارجاع برای ECT/کتامین طبق راهنماهای کشوری.
اصل: هر تغییر باید مستند باشد (شدت، پالس، هدف، پاسخ/تحمل).
5) بوستر و نگهدارنده (Maintenance)
برای چه کسانی؟
بیمارانی که پاسخ خوب/رِمیشن گرفتهاند ولی سابقهٔ عود دورهای دارند (MDD عودکننده، الگوهای فصلی، استرسورهای پیشبینیپذیر).
مدلهای رایج برنامهریزی
هفتهای ۱ جلسه × ۴ هفته → یکهفتهدرمیان × ۸ هفته → ماهانه (در صورت پایداری).
Symptom-Triggered: با اولین بازگشت علائم (مثلاً +۴ امتیاز PHQ-9 یا الگوی خواب/انرژی بد) ۱–۳ جلسهٔ بوستر پشتسرهم.
اجرای بوستر
همان هدف/پروتکل/شدت که بیمار با آن پاسخ گرفته است (تغییر فقط با دلیل).
اگر علامت برگشت کرد: بوستر سنگینتر (۲–۳ روز پیاپی) و سپس برگشت به برنامهٔ نگهدارنده.
6) پایان دوره (Fade-out) و کاهش تدریجی
خیلی از مراکز در ۱–۲ هفتهٔ آخر، دفعات را ۳→۲→۱ جلسه/هفته کم میکنند تا گذار نرم باشد.
همزمان پلان نگهدارنده و «شرایط بازگشتِ سریع» را به بیمار آموزش دهید.
7) پایش و گزارشِ نتیجه (Outcome Tracking)
هفتگی: PHQ-9 (یا ابزار پایهی شما) + یادداشت خواب/انرژی/عملکرد.
پایان دوره: همان ابزار + CGI-I؛ نمودار روند را به بیمار نشان دهید (افزایش ادراک کارآمدی درمان).
پیگیری ۴–۸ هفتهای: بررسی نیاز به بوستر/تنظیم دارو/رواندرمانی.
8) KPIهای کلینیک (برای بهبود مستمر)
نرخ پاسخ (%≥50٪ کاهش) | نرخ رِمیشن | میانگین تغییر PHQ-9
میانگین جلسات تا پاسخ | نرخ عدمپاسخ و مسیر جایگزین
نرخ عوارض (سردرد/تحمل/سنکوپ) | انضباط لوکالیزیشن (انحراف زاویه/نقطه)
9) دو الگوی آمادهٔ «کارت اتاق» (Room Card)
الف) کارت تصمیم میانهٔ دوره (جلسهٔ 10–12)
ΔPHQ-9 = __٪ (هدف ≥20٪؟)
لوکالیزیشن/زاویه/شدت/پالس تأیید شد □
عارضهٔ محدودکننده؟ سردرد □ اضطراب □ تحمل خوب □
اگر Δ<20٪ → گام A (rMT مجدد، شدت +۵٪، پالس کامل) → بازبینی هفتهٔ بعد
ب) کارت بوستر/نگهدارنده
طرح: هفتگی ×۴ → دوهفتهیکبار ×۸ → ماهانه
معیار شروع بوستر: PHQ-9 +۴ یا بازگشت شاخصهای شخصی
بوستر: __ جلسه پشتسرهم | پروتکل: همان پروتکل پاسخدهنده
ارزیابی پس از بوستر: PHQ-9 / CGI-I / خواب / عملکرد
مستندسازی، رضایت آگاهانه، SOP و مدیریت کیفیت در درمان rTMS
این بخش به شما یک «پکیج اجرایی» میدهد تا درمان rTMS را از نظر قانونی، اخلاقی و عملیاتی بینقص اجرا و مستند کنید. هر مورد را میتوانید عیناً در کلینیک پیادهسازی کنید.
1) چکلیست مستندسازی پرونده (قبل، حین و بعد از درمان)
الف) پیش از شروع (Intake)
شرح حال روانپزشکی کامل + تشخیصهای DSM-5-TR
سوابق درمان (دارو، رواندرمانی، ECT، کتامین، TMS قبلی)
غربالگری خطر تشنج/موارد منع نسبی یا مطلق (سابقه تشنج، ضایعه مغزی، ایمپلنتهای فلزی/الکترونیکی، بارداری، …)
ارزیابی ایدههای خودآسیبی/خودکشی (C-SSRS) و برنامه ایمنی
آزمونهای پایه علائم: PHQ-9 / BDI-II (افسردگی)، GAD-7 (اضطراب)، Y-BOCS (وسواس)، PSQI (خواب)
ارزیابی شناختی کوتاه (در صورت نیاز): MoCA یا T-MOCA
معاینه عصبی کوتاه + خط پایه فشارخون/نبض
رضایت آگاهانه rTMS (امضا + تاریخ)
تصمیم درمانی و نقشه پروتکل (هدف، نیمکره، فرکانس، شدت، تعداد پالس، جلسات/هفته، طول دوره)
ب) شروع دوره (Session 1)
Motor Threshold (MT) تعیینشده: روش (RMT/AMT)، محل، تعداد پاسخها، مقدار نهایی (%MSO)
فیتینگ و ثبت محل هدفگیری: 5 سانتیمتر، Beam F3، یا Neuronavigation (اسکرینشات/مختصات ذخیره شود)
پروتکل نسخه 1 (V1): مثال: 10Hz-L-DLPFC، 3000 پالس، 120% RMT، 37.5 دقیقه
آموزش بیمار: عوارض مورد انتظار، نکات ایمنی، تماس اضطراری
ج) پیگیری روزانه جلسات (Session Notes)
برای هر جلسه یک سطر/یادداشت کوتاه:
شماره جلسه، تاریخ، ساعت
شدت (%MT)، تعداد پالس، الگوی قطار/استراحت، پروتکل (10Hz، 1Hz، iTBS…)
تلورانس/عوارض (VAS درد ناحیه، سردرد، اضطراب، سنکوپ و…)
تغییرات دارویی، کیفیت خواب، بحران روانی بین جلسات
تنظیمات انجامشده (بهویژه اگر دز/هدف تغییر کرده)
امضای تکنسین/ناظر
د) ارزیابیهای هفتگی
PHQ-9 ،GAD-7 (± Y-BOCS) با نمودار روند
گزارش ذهنی بیمار (SUDS، انرژی، خواب، اشتها، عملکرد اجتماعی)
تصمیمات دستکاری پروتکل (Dose/Target/Pattern) + مستندات دلیل بالینی
هـ) پایان دوره و فالوآپ
تکرار کامل مقیاسها + تعریف پاسخ (≥50% کاهش) و بهبودی (PHQ-9 ≤ 4 یا BDI-II ≤ 10)
گزارش نهایی درمان + برنامه بوستر/نگهدارنده
نامه به ارجاعدهنده/پرونده الکترونیک: پروتکل اجرا شده، ایمنی، نتایج، توصیههای بعدی
2) رضایت آگاهانه (نکات کلیدی که باید حتماً باشد)
ماهیت درمان: غیرتهاجمی، استفاده از میدانهای مغناطیسی مکرر برای تعدیل شبکههای مغزی
منافع مورد انتظار: کاهش علائم (افسردگی/اضطراب/وسواس…)، بهبود عملکرد
خطرات/عوارض شایع: درد پوست سر، سردرد، انقباض عضلات صورت/فک، خستگی گذرا
خطرات نادر ولی مهم: تشنج (بسیار نادر)، سنکوپ وازووگال، تغییرات خلقی
جایگزینها: دارو، رواندرمانی، ECT/کتامین، عدم درمان
شرایط قطع/تعلیق: بارداری، تشنج، علائم مانیا/هیپومانیا، عوارض غیرقابلتحمل
حریم خصوصی و دادهها: ذخیره دادههای درمانی و امکان استفاده پژوهشی با رضایت جداگانه
حق انصراف: در هر زمان، بدون لطمه به سایر خدمات
امضاها: بیمار/قیم، پزشک/تکنسین، تاریخ
3) SOPهای حیاتی کلینیک rTMS (Standard Operating Procedures)
ایمنی و مدیریت بحران
غربالگری پیش از درمان + چکلیست ورود هر جلسه (تغییر دارو، بیخوابی شدید، مصرف الکل/مواد)
کیت اورژانس: ماسک جیبی، آتروپین/لیدوکائین نیاز نیست، ولی فشارسنج/پالساکس/گلوکومتر باید باشد
پروتکل مدیریت تشنج: توقف فوری، حفاظت سر، تماس اورژانس، مستندسازی دقیقهبهدقیقه
آموزش CPR پایه به تیم، مانیتورینگ علائم حیاتی وقتی اندیکه است (مثلاً در سالمندان/بیماریهای قلبی)
کالیبراسیون و نگهداری دستگاه
بررسی روزانه کابل/Coil و فنها، ثبت Hours Counter کویل، تمیزکاری
Warm-up طبق دستور سازنده، پیگیری خطاهای سیستم (Error Logs)
تست هفتگی Output Consistency (در صورت داشتن Power Meter یا Phantom)
تعویض کویل بر اساس ساعت مصرف/افت کارایی (سند و امضا)
استاندارد تعیین MT و هدفگیری
روش یکسان (Rossini-Rothwell) با معیار «۵ پاسخ از ۱۰ تحریک»
ثبت مختصات/فاصله کلاه (Cap Size) و نگاشت Beam F3 (در صورت نبود ناوبری)
Re-MT: حداقل هفتگی یا با تغییرات بالینی/دارویی یا عدم تحمل
دزینگ ایمن و تنظیمات
حداکثر 120–130% RMT برای بیشتر پروتکلهای 10Hz
فاصله قطار/استراحت طبق گایدلاینها (جلوگیری از بار بیشازحد تجمعی)
TBS: iTBS/cTBS با مجموع 600 پالس (رایج)، 80% AMT یا 100% RMT برحسب دستگاه/راهنما
حفظ محرمانگی و مدیریت داده
پرونده الکترونیک با دسترسی سطحبندی، نسخه پشتیبان رمزگذاری شده
داشبورد نتایج (Outcome Dashboard) برای پایش نرخ پاسخ/بهبودی و عوارض
4) نکات حقوقی/اخلاقی مهم
شفافیت در وعده درمان: rTMS «درصدی از بیماران» را پاسخگو میکند، «درمان تضمینی ۱۰۰٪ نیست».
رسیدگی به آسیبپذیرها: نوجوانان، سالمندان، بارداری، مانیا/روانپریشی — فقط با اندیکاسیون و نظارت متخصص.
تعارض منافع: در مواد آموزشی/بازاریابی، مرجع علمی و محدودیتها ذکر شود.
دسترسی عادلانه: سیاست تخفیف/برنامه اقساط برای موارد واجد شرایط (در صورت امکان).
5) چکلیست آمادهسازی اتاق rTMS (Daily Room Readiness)
کویل سالم و محکم | کابلها بدون لهیدگی
صندلی/هدریست تنظیم و ثابت | Earplugs موجود
کارت اضطراری، شمارههای تماس، کیت کمکهای اولیه
دستگاه روشن، فنها کار میکنند، خطای سیستم ندارد
پوشه جلسه امروز آماده (لیست بیماران، پروتکلها، فرم علائم)
پایش پاسخ، پیشبینیکنندهها و مدیریت «عدمپاسخ» در rTMS
هدف این بخش: بدانیم چطور زود و دقیق بفهمیم درمان دارد کار میکند، چه عواملی پاسخ را بهتر/بدتر میکند، و اگر پاسخ کافی نبود گامبهگام چه تنظیماتی انجام دهیم.
1) تعریف پاسخ و زمانبندی ارزیابی
پاسخ (Response): ≥ 50% کاهش در نمرهٔ مقیاس هدف (مثلاً PHQ-9/BDI-II برای افسردگی، GAD-7 برای اضطراب، Y-BOCS برای وسواس).
بهبودی (Remission): رسیدن به آستانهٔ پایین (مثلاً PHQ-9 ≤ 4 یا BDI-II ≤ 10).
زمانبندی ارزیابی:
Baseline قبل از جلسهٔ اول
هفتگی (ترجیحاً روز اول هر هفته درمان)
پایان دوره و Follow-up (۴ و ۱۲ هفته بعد)
علاوه بر نمرهٔ مقیاسها، شاخصهای عملکردی را ثبت کنید: خواب، انرژی، تمرکز، کارکرد اجتماعی، کار/تحصیل.
2) پیشبینیکنندههای پاسخ بهتر (بهصورت عملیاتی)
پایبندی بالا به جلسات (عدم غیبت و وقفه)، خواب کافی، عدم مصرف الکل/مواد.
شدت و مدت بیماری کمتر و مقاومت درمانی پایینتر (TRD سطح پایینتر).
ثبات دارویی (عدم تغییرات متوالی در وسط دوره) و پرهیز از بنزودیازپینهای دوز بالا نزدیک به جلسه.
هدفگیری دقیقتر قشر پیشپیشانی پشتی-جانبی (DLPFC) با Beam F3 یا Neuronavigation.
مدیریت درد/اضطراب سرجلسه (تا بیمار دوز کافی را تحمل کند).
نکته: وجود همبودهایی مثل بیخوابی شدید، اضطراب کنترلنشده، مصرف مزمن بنزوها و مصرف الکل/مواد، پاسخ را کاهش میدهد—سریعاً اصلاحشان کنید.
3) اگر پاسخ ناکافی بود، از هفتهٔ ۲ تا ۳ چه کنیم؟
معیار هشدار زودهنگام: اگر تا جلسهٔ ۱۰ (تقریباً هفتهٔ دوم) <20% بهبود دیده شد، وارد مسیر بهینهسازی شوید:
بازسنجی MT و کیفیت هدفگیری
MT را حداقل هفتگی یا با هر تغییر بالینی/دارویی دوباره بگیرید.
محل کویل را با Beam F3 یا ناوبری چک و عکس/مختصات را ثبت کنید.
زاویهٔ کویل را ثابت نگه دارید (Chin rest/Headband) تا پراکندگی میدان کم شود.
افزایش شدت (Intensity) در صورت تحمل
برای 10Hz-L-DLPFC: از 110–120% به 120–130% RMT برسانید (پلهای و با کنترل درد/سردرد).
افزایش پالس یا طول دوره
پالس روزانه: از 3000 به 3500–4000 پالس (اگر دستگاه/گایدلاین شما اجازه میدهد).
طول دوره: از 20–30 جلسه به 30–36 جلسه افزایش دهید.
تغییر یا افزودن هدف/الگو
دوطرفه: ادامهٔ 10Hz چپ + 1Hz راست (در اضطراب/تحریکپذیری مفید است).
یا Dual-Mode: 10Hz چپ + iTBS راست (600 پالس).
در عدم تحمل 10Hz: iTBS چپ (شلیک سریع 3 دقیقهای) را جایگزین کنید.
مدیریت درد/اضطراب برای تحمل دز بالاتر
پیش از جلسه استامینوفن/ایبوپروفن (در صورت عدم منع)، ژل لیدوکائین موضعی، رَمپ تدریجی شدت.
آموزش و تنفس آهسته برای کاهش اضطراب؛ از بنزوها نزدیک جلسه پرهیز کنید.
4) ترکیب با درمانهای کمکی (Augmentation)
دارودرمانی بهینه: SSRI/SNRI مناسب، بپروپیون/میرتازاپین بسته به پروفایل؛ ثبات را حفظ کنید.
رواندرمانی (CBT/BA/ACT) همزمان با rTMS—ترجیحاً همروز یا فردای جلسه تا از پنجرهٔ پلاستیسیتهٔ عصبی بهره ببرید.
بهداشت خواب، نور روز، ورزش هوازی ملایم، تغذیهٔ منظم—روی همه تکلیف خانگی بدهید.
5) الگوریتم عملی ۴ هفتهٔ اول (افسردگی MDD بهعنوان نمونه)
هفته 1:
پروتکل پایه: 10Hz-L-DLPFC، 3000 پالس، 110–120% RMT
آموزش کامل + مدیریت درد/گوشگیر + ارزیابی Baseline
هفته 2 (جلسه 6–10):
ارزیابی: اگر ≥20% بهبود → ادامه.
اگر <20% → Re-MT + تصحیح هدف + فکر به افزایش شدت/پالس.
هفته 3:
در عدم بهبود کافی:
شدت تا 120–130%،
بررسی دوطرفه/Dual-Mode،
افزایش پالس تا 3500–4000،
افزودن iTBS راست یا جایگزینی با iTBS چپ.
هفته 4:
اگر روند رو به بهبود است → تمدید دوره تا 30–36 جلسه.
اگر عدم پاسخ معنیدار باقی است → بازنگری تشخیص/همبودها، بررسی مسیرهای جایگزین (Esketamine/ECT) و ارجاع.
6) معیارهای توقف/تغییر خط درمان
بدترشدن واضح علائم (افکار خودآسیبی فعال، مانیا/روانپریشی تازه).
عدم هرگونه پاسخ بالینی پس از ۳۰–۳۶ جلسه با تنظیمات مناسب.
عوارض غیرقابلتحمل علیرغم مداخلات تسکینی.
در این سناریوها، جلسهٔ Case Conference بگذارید و مسیر جایگزین را با بیمار بهصورت رضایت آگاهانه جدید مرور کنید.
7) نکات طلایی تیمی
یک تغییر در هر بار: برای فهم اثر آن تغییر، چند جلسه با همان تنظیم جلو بروید.
گزارش روند هفتگی با نمودار ساده (PHQ-9/GAD-7) در پرونده چاپ بچسبانید.
ثبات زاویه/محل کویل مثل شدت مهم است—بهخصوص در پروتکلهای فرکانس بالا و iTBS.
کیفیت تعامل با بیمار (اطمینان، آموزش، پاسخ به نگرانیها) خودش یک مُضاعِف اثربخشی است.
ایمنی، عوارض شایع و مدیریت آنها در rTMS
هدف این بخش: شناخت ریسکها و عوارض محتمل، پیشگیری فعال، و الگوریتمهای عملی مدیریت هر عارضه تا درمان ایمن، پایدار و مؤثر باقی بماند.
1) اصول پایهٔ ایمنی
غربالگری قبل از شروع: تشنج/سابقه صرع، ضایعه ساختاری مغز، TBI متوسط/شدید، دوقطبی/مانیا، ایمپلنتها و اجسام فلزی/الکترونیکی نزدیک میدان، بارداری، داروهای کاهنده آستانه تشنج (مثلاً بوپروپیون دوز بالا، ترامادول، کلوزاپین).
پرهیز از افزایش ریسک روزانه: بیخوابی شدید، مصرف الکل/مواد ۴۸–۲۴ ساعت اخیر، تغییر خودسرانهٔ دارو.
حفاظت شنوایی: گوشگیر مناسب برای بیمار و درمانگر؛ تطابق صحیح و ثبت در پرونده.
ثبات فنی جلسه: زاویه و محل کویل ثابت، ثبت مختصات، کنترل دمای کویل/استراحت مناسب بین ترنها، رعایت Duty Cycle دستگاه.
2) عوارض شایع و مدیریت قدمبهقدم
الف) سردرد/درد پوست سر
پیشگیری: Ramp تدریجی شدت، پیشدرمانی با استامینوفن/ایبوپروفن در صورت نیاز، کلاه/پد نرم زیر کویل، چک تماس الکترود Earthing (اگر لازم).
مدیریت: شدت را موقتاً یک پله کم کنید، زاویه تماس را اندکی اصلاح کنید، وقفهٔ کوتاه دهید؛ در سردردهای مکرر پروفیلاکسی ساده (پس از مشورت پزشک).
علایم هشدار: سردرد غیرمعمول شدید/پیشرونده، نورولوژیک فوکال → ارزیابی پزشکی قبل از ادامه.
ب) اضطراب/بیقراری/بیخوابی
پیشگیری: آموزش قبل از شروع (انتظار حسی حین TMS)، تکنیک تنفس آهسته، زمانبندی جلسات در ساعات اولیه روز.
مدیریت: مکث کوتاه، کاهش ملایم شدت، آموزش مجدد؛ از بنزودیازپین نزدیک جلسه پرهیز (ممکن است پاسخ درمانی را کاهش دهد).
تعدیل پروتکل: در اضطراب بالینی بالا، افزودن ۱Hz راست یا ترکیب دوطرفه میتواند مفید باشد.
ج) واکنش وازوواگال (سرگیجه/سنکوپ)
اقدام فوری: توقف درمان، وضعیت ایمن (در صورت نیاز Trendelenburg ملایم)، پایش فشار/نبض، اطمینانبخشی.
پیشگیری جلسه بعد: هیدراسیون مناسب، میانوعده سبک، حذف عوامل استرسزا (ترس از سوزن/خون)، شروع با شدت پایین و رَمپ.
د) وزوز گوش/حساسیت شنوایی
پیشگیری: گوشگیر استاندارد با فیت مناسب؛ آموزش الزام استفاده.
مدیریت: بررسی فیت گوشگیر، کاهش اندک شدت؛ در علایم پایدار، ارجاع ارزیابی شنوایی.
3) رویدادهای نادر و مهم
تشنج وابسته به TMS (بسیار نادر)
اقدام حین واقعه:
کویل را سریع کنار بگذارید و تجهیزات را دور کنید.
ایمنی راه هوایی؛ بیمار را به پهلو بخوابانید، سر را محافظت کنید.
زمانسنجی مدت تشنج؛ محیط را خلوت و ایمن کنید.
اگر >۵ دقیقه یا خوشهای/اولین تشنج زندگی/تروما → EMS/اورژانس.
پس از پایان: علایم حیاتی، ارزیابی نورولوژیک مختصر، ثبت کامل رویداد، اطلاع به روانپزشک/نورولوژیست.
بازگشت به درمان: پس از ارزیابی پزشک؛ اصلاح عوامل خطر (خواب، الکل/مواد، داروها)، بازسنجی MT، کاهش شدت/پالس، یا تغییر الگو (مثلاً از 10Hz به iTBS با نظارت). گاهی تعلیق موقت منطقی است.
مانیا/هایپومانیا در بیماران دوقطبی
پیشگیری: اسکرین اولیه دقیق، پوشش تثبیتکننده خلق، شروع محافظهکارانه.
مدیریت: در صورت ایجاد علایم مانیا، وقف درمان تحریککننده، ارزیابی روانپزشکی، تنظیم دارو؛ در صورت نیاز جایگزینی با ۱Hz راست پس از کنترل مانیا.
4) چه زمانی «جلسه را متوقف» یا «کل دوره را بازنگری» کنیم؟
بدترشدن واضح خلق/سایکوز/افکار خودآسیبی فعال.
سردرد یا درد غیرقابلتحمل علیرغم تعدیلات.
رویداد وازوواگال تکرارشونده با خطر ایمنی.
عدم پاسخ معنادار پس از ۳۰–۳۶ جلسه با تنظیمات بهینه → Case Conference و بررسی گزینههای جایگزین (Esketamine/ECT/تغییر تشخیص/کاموربیدیتیها).
5) عوامل کاهنده اثربخشی (و کارهایی که باید انجام دهیم)
بیخوابی/اختلال خواب: بهداشت خواب، زمانبندی جلسات، درمان بیخوابی.
الکل/مواد: قطع، فاصله امن ۴۸–۲۴ ساعت، حمایت ترک.
بنزودیازپین دوز بالا/نزدیک جلسه: کاهش تدریجی با نظر پزشک.
تغییرات پیدرپی دارویی وسط دوره: ثبات تا حد ممکن؛ تغییرات غیرضروری را به پس از دوره موکول کنید.
هدفگیری نامنظم/زاویه ناپایدار: استفاده از Beam F3/ناوبری، فیکسکردن سر، عکس و مختصات هر جلسه.
6) چکلیست ایمنی روزانه (پیشنهادی برای نصب کنار دستگاه)
گوشگیر بیمار و درمانگر چک شد.
غربالگری همانروزی: قطع/تغییر دارو؟ بیخوابی شدید؟ الکل/مواد؟
محل/زاویهٔ کویل با مختصات جلسه قبل مقایسه و تأیید شد.
MT بهروز است (تغییرات بالینی/دارویی؟ بله/خیر).
دمای کویل و استراحت بین ترنها رعایت شد.
ثبت دوز/پالس/تحملپذیری و عوارض انجام شد.
نمرهٔ هفتگی (PHQ-9/GAD-7/Y-BOCS) در روز اول هفته ثبت شد.
7) مستندسازی کوتاه (الگوی یادداشت روزانه)
پروتکل/هدف: (L-DLPFC 10Hz 3000 pulses @120% RMT / iTBS …)
MT: امروز …%؛ آخرین تغییر دارویی: … / ندارد
تحمل: خوب / متوسط / ضعیف (سردرد خفیف/متوسط/شدید؛ درد پوست سر؛ اضطراب)
اقدامات تسکینی: استامینوفن، اصلاح زاویه/پد، Ramp، مکثها
عوارض غیرمعمول: ندارد / شرح مختصر و اقدام
برنامه جلسه بعد: ادامه بدون تغییر / افزایش شدت / افزایش پالس / تغییر الگو / ارجاع
سفارشیسازی پروتکلها برای اختلالات مختلف
هدف: برای هر اختلال، «هدفگذاری»، «الگوی تحریک»، «دوز پیشنهادی»، «تعداد جلسات»، «شاخصهای پایش»، و «مسیر بهینهسازی اگر پاسخ ناکافی بود» را بدهیم. گزینهها را برای کویل Figure-8 و در صورت دسترسی، دیپکویل (H7/H4/DB-80) هم میدهم.
اصول مشترک دوزدهی (یادآوری سریع)
iTBS کلاسیک: 600 پالس، ~3 دقیقه، معمولاً 80% RMT (یا % of AMT بسته به دستگاه/گایدلاین).
10Hz چپ DLPFC: 3–4 ثانیه ON / 26–27 ثانیه OFF، 3000 پالس، 110–120% RMT (قابل افزایش تا 130% با تحمل).
1Hz راست DLPFC/SMA: 900–1800 پالس، 100–110% RMT.
جلسات: 20–30 (قابل تمدید تا 36)؛ پاسخ دیرهنگام → ادامه تا 40 با منطق بالینی.
پایش هفتگی: PHQ-9/BDI-II (افسردگی)، GAD-7 (اضطراب)، Y-BOCS (OCD)، PCL-5 (PTSD)، ASRS/IVA-2 (ADHD)، HIT-6/MPQ (درد/میگرن).
Trigger بهینهسازی: <20% بهبود تا جلسه 10 → بازسنجی MT/هدف، افزایش شدت/پالس یا تغییر الگو.
افسردگی MDD/TRD
هدف اصلی: چپ DLPFC (افزاینده شبکه کنترل/خلق).
Primary (Figure-8):
گزینه A: 10Hz چپ DLPFC | 3000 پالس | 110–120% RMT | 25–30 جلسه
گزینه B: iTBS چپ DLPFC | 600 پالس | 80% RMT | 20–30 جلسه (سریعتر، تحمل بهتر)
Augment/Alternate:
Bilateral: 1Hz راست (900–1200) → سپس 10Hz چپ (3000)
Dual-Mode: iTBS راست (600) + iTBS چپ (600) یا iTBS راست + 10Hz چپ
Deep-coil (اگر H7/DB-80 دارید):
mPFC/ACC (H7) پروتکلهای تاییدشده برای خلق/وسواس؛ در افسردگی مقاوم میتواند Adjunct باشد.
بهینهسازی اگر پاسخ ناکافی: افزایش به 120–130%، افزایش پالس تا 3500–4000، تغییر به دوطرفه، افزودن CBT/BA، بهداشت خواب، پرهیز از بنزو نزدیک جلسه.
وسواس (OCD)
هدفهای کلیدی: SMA/Pre-SMA (مهاری) و/یا mPFC/ACC (دیپ).
Primary (Figure-8):
1Hz دوطرفه SMA | 1200–1800 پالس هر سمت | 100–110% RMT | 25–30 جلسه
میتوانید iTBS چپ DLPFC (600) را بهعنوان تقویت تنظیم خلق/کنترل شناختی اضافه کنید.
Deep-coil (H7 – mPFC/ACC):
پروتکل H7 اختصاصی OCD (جلسات 25–30). در صورت دسترسی، ترجیح دارد.
پایش: Y-BOCS هفتگی، ثبت اجبار/وسواس هدف، تکلیف ERP/CBT همزمان.
بهینهسازی: اگر <20% تا جلسه 10 → افزایش پالس SMA، افزودن DLPFC، یا سوئیچ به H7 (در صورت دسترسی).
اضطراب (GAD/اجتماعی/پانیک)
هدف: R-DLPFC مهاری برای کاهش بیشبرانگیختگی، سپس تقویت شبکه تنظیم از چپ.
Primary (Figure-8):
1Hz راست DLPFC | 1200–1800 پالس | 100–110% RMT | 20–30 جلسه
در صورت خلق پایین همراه: iTBS چپ DLPFC (600) بهعنوان Adjunct
Alternate: Bilateral sequential (1Hz راست → 10Hz چپ).
پایش: GAD-7، PSQI (خواب).
نکته: از بنزوهای دوز بالا نزدیک جلسه پرهیز؛ آموزش تنفسی/ACT کنار درمان.
PTSD
وضعیت شواهد: نویدبخش، اما ناهمگون؛ معمولاً R-DLPFC مهاری یا Bilateral.
Primary (Figure-8):
1Hz راست DLPFC | 1200–1800 | 20–30 جلسه
یا iTBS چپ DLPFC در بیماران با خلق پایین غالب.
Deep-coil (H7/mPFC): مفید در برخی پروتکلها (بسته به دسترس).
پایش: PCL-5 + خواب/کابوس (ISQ)؛ همزمان Trauma-focused CBT/EMDR اگر امکانش هست.
احتیاط: اگر تحریکپذیری/بیخوابی تشدید شد → کاهش شدت/تغییر الگو به 1Hz راست.
درد مزمن / میگرن
هدف: M1 کنترا-لترال ناحیه درد (افزایشی)؛ در میگرن پروتکلهای ویژه.
Primary (Figure-8):
10–20Hz M1 | 1500–2000 پالس | 90–110% RMT | 10–15 جلسه (2–3/هفته)
میگرن: برخی دستگاهها Single-pulse TMS یا iTBS M1 را پشتیبانی میکنند.
پایش: NRS/VAS درد، HIT-6، کاهش مصرف مُسکن.
نکته: تمرینات کششی/فیزیوتراپی موازی، تنظیم خواب/استرس.
ADHD (کودک/بزرگسال)
هدفها: rDLPFC مهاری (کاهش تکانشگری) یا lDLPFC افزایشی (بهبود توجه/WM).
Primary (Figure-8):
iTBS چپ DLPFC (600) | 80% RMT | 20–25 جلسه
یا 1Hz راست DLPFC | 1200–1500 | 20–25 جلسه
کودکان: شدت محافظهکارانه، زمان کوتاهتر، همکاری والدین؛ همیشه رضایت آگاهانه تقویتشده. بسته به گایدلاین کشوری.
پایش: ASRS (بزرگسال) / IVA-2، CANTAB شاخصهای توجه/WM.
وابستگی به نیکوتین (Smoking Cessation)
Deep-coil (H4 – prefrontal-insular) دارای تأیید در برخی سامانهها.
اگر Figure-8: میتوان lDLPFC iTBS را با مداخلات ترک (NRT/وارنیکلین/CBT) ترکیب کرد؛ شواهد ضعیفتر از H4.
پایش: CO بازدم، تعداد سیگار روزانه، پرسشنامه اشتیاق (QSU-Brief).
برنامه: 15–18 جلسه + تقویتهای هفتگی اوایل ترک.
بیخوابی (Insomnia) – Adjunct
هدف: rDLPFC 1Hz یا SMA 1Hz (کاهش برانگیختگی)، زمانبندی جلسات در صبح.
پایش: ISI/PSQI، Sleep diary.
ترکیب: CBT-I، نورروزمانی (نور صبح)، بهداشت خواب.
دوقطبی (افسردگی) – با احتیاط
ترجیح: 1Hz راست DLPFC یا iTBS چپ با شدت محافظهکارانه فقط با پوشش تثبیتکننده خلق.
پایش مانیا: YMRS هفتگی؛ هر نشانه مانیا → توقف پروتکل افزایشی و ارزیابی.
نگهدارنده/بوستر (پس از پاسخ)
هفته 1–4 پس از اتمام دوره: 1–2 جلسه/هفته (کاهش پلکانی)
ماه 2–3: هر 1–2 هفته یکبار
بعد از آن: PRN مبتنی بر علائم یا 1 جلسه/ماه برای پایدارسازی
در OCD/PTSD، استمرار رواندرمانی و ERP کلیدی است.
جمعیتهای خاص، احتیاطات تخصصی + SOP و «رضایت آگاهانه» کوتاه rTMS
هدف: اجرای rTMS ایمن و مؤثر در موقعیتهای ویژه (سالمندان، بارداری/شیردهی، صرع کنترلشده، TBI/سکته، درد نوروپاتیک، ایمپلنتها/فلزات) و فراهمکردن رویهٔ استاندارد (SOP) و فرم رضایت کوتاه برای کلینیک.
۱) اصول طلاییِ ایمنی در جمعیتهای خاص
ثبات خواب/دارو را قبل و حین دوره حفظ کنید؛ الکل/مواد = پرهیز ۴۸–۲۴ ساعت.
MT را در این گروهها زودتر و مکررتر بازسنجی کنید (حداقل هفتگی یا با هر تغییر بالینی/دارویی).
هدفگیری پایدار (Beam F3 یا ناوبری) و زاویهٔ ثابت کویل بهاندازهٔ شدت مهم است.
گوشگیر استاندارد برای بیمار و درمانگر الزامی است.
۲) سالمندان (≥۶۵ سال)
ریسک/ویژگیها: تحمل پوست سر کمتر، چنددارویی، نوسان MT بهعلت آتروفی/دارو.
پروتکلمحور:
شروع محافظهکارانه (10Hz چپ 110% RMT یا iTBS چپ 80% RMT)، Ramp تدریجی.
مسکن ساده/پد نرم برای پوست سر؛ جلسات صبحگاهی (همراستا با ریتم زیستی).
پایش هفتگی PHQ-9/GAD-7 + شاخصهای عملکردی (خواب/تعامل اجتماعی/انرژی).
بهینهسازی: اگر <20% بهبود تا جلسه ۱۰ → Re-MT، تصحیح هدف، افزایش شدت به 120–130% در صورت تحمل.
۳) بارداری و شیردهی
ایمنی کلی: دادههای موجود rTMS را در بارداری «نسبتاً ایمن» نشان میدهند (بهویژه افسردگی بارداری/پسازایمان).
احتیاطات:
اخذ تأیید متخصص زنان؛ ارزیابی خطر–فایده.
وضعیت نشسته با پشتی مناسب؛ پرهیز از Hypotension در حالت طاقباز.
گوشگیر دقیق؛ کاهش اضطراب با آموزش.
دارو: ترجیحاً ثبات رژیم؛ شیردهی: rTMS تداخل مستقیم ندارد.
پروتکلهای پیشنهادی: iTBS چپ (۳ دقیقه) یا 10Hz چپ با شدت محافظهکارانه؛ جلسههای کوتاهتر و استراحتهای بیشتر.
۴) صرع کنترلشده / آستانهٔ تشنج پایین
اصل: rTMS منع مطلق نیست؛ اما احتیاط سطح بالا.
پیشگیری:
عدمِ محرومیت از خواب، پرهیز الکل/مواد، ادامهٔ داروی ضدصرع طبق نسخه.
شروع با الگوی محافظهکارانه (۱Hz راست یا iTBS چپ با نظارت)، افزایش پلهای شدت.
آمادگی اورژانس: پروتکل تشنج (بخش SOP) + تیم آگاه.
تعدیل دارویی: پرهیز/احتیاط با داروهای کاهندهٔ آستانه تشنج (بوپروپیون دوز بالا، کلوزاپین، ترامادول، ترکیب چند محرک CNS).
بهینهسازی: پاسخ ناکافی → افزایش تدریجی شدت/پالس با حفظ ایمنی؛ در تشدید ریسک، تغییر الگو به ۱Hz.
۵) آسیب مغزی تروماتیک (TBI) / سکته (CVA)
خطر: ضایعهٔ ساختاری = آستانه تشنج متغیر.
غربالگری: شرح حال دقیق + تصویربرداری اخیر (در صورت دسترس)؛ تشنج قبلی؟ نقص فوکال؟
پروتکلمحور:
فاز مزمن/پایدار: امکان درمان افسردگی پس از TBI با پروتکلهای استاندارد (محافظهکارانه شروع کنید).
سکته: بسته به ضایعه، هدفگیری DLPFC برای خلق/توجه؛ برای درد/اسپاستیسیتی، M1 با احتیاط.
پایش نزدیک: MT هفتگی؛ عوارض سردرد/سرگیجه → کاهش شدت/وقفه/ارزیابی نورولوژی.
۶) درد نوروپاتیک / میگرن
M1 (کنترا-لترال به سمت درد): 10–20Hz | 1500–2000 پالس | 90–110% RMT | 10–15 جلسه.
میگرن: برخی سامانهها Single-Pulse یا iTBS دارند؛ گوشگیر دقیق، جلسات صبح.
Adjunct: فیزیوتراپی/ورزش سبک/بهداشت خواب؛ پایش NRS/HIT-6 + مصرف مُسکن.
۷) ایمپلنتها و فلزات
منع نسبی/مطلق نزدیک میدان:
کاشت حلزون گوش، کاشت عمقی مغز (DBS)، پمپهای قابل برنامهریزی نزدیک سر → نیازمند استعلام سازنده/متخصص مربوطه؛ غالباً اجتناب از تحریک نزدیک دستگاه.
پیسمیکر/ICD: تداخل بعید در فاصلهٔ DLPFC، اما کاردیولوژی Clearance + احتیاط (کویل را از مسیر لیدها دور نگه دارید).
فلزات غیرمغناطیسی (تیتانیوم/دندانی): معمولاً ایمن.
قاعدهٔ عملی: اگر نوع/مکان ایمپلنت نامشخص است → درمان را به تعویق بیندازید تا مدرک سازگاری فراهم شود.
۸) داروها و فاکتورهای مؤثر بر اثربخشی
کاهش پاسخ: بنزودیازپینهای دوز بالا نزدیک جلسه، الکل/مواد، بیخوابی شدید، تغییرات پیاپی دارویی.
افزایش ریسک تشنج: بوپروپیون دوز بالا، کلوزاپین، ترامادول، برخی ضدافسردگیهای سهحلقهای در دوز بالا؛ تداخل چندگانهٔ محرکها.
سیاست: حد امکان ثبات دارو در دورهٔ rTMS؛ تغییرات ضروری → مستندسازی + Re-MT.
۹) تعدیل دوز/الگو در جمعیتهای خاص (راهنمای سریع)
تحمل پایین درد پوست سر: iTBS چپ یا 10Hz با Ramp طولانیتر + پد نرم + مسکن ساده.
اضطراب بالا/بیخوابی: ۱Hz راست (± iTBS چپ)؛ جلسات صبح؛ مداخلات ذهنآگاهی.
آستانهٔ تشنج پایین/صرع کنترلشده: شروع با ۱Hz راست / iTBS چپ محافظهکارانه؛ افزایش آهستهٔ شدت.
سالمند چنددارویی: جلسات کوتاهتر، Re-MT هفتگی، پایش دقیق فشار/سرگیجه.
برنامه «بوستر/نگهدارنده» پس از rTMS + Recall و پیگیری ۳–۶ ماهه + فرم خروج یکصفحهای
هدف: پیشگیری از بازگشت علائم با برنامههای نگهدارنده استاندارد برحسب اختلال، الگوریتم Recall (فراخوانِ به-موقع در شروعِ عود)، و یک فرم خروج آماده چاپ که تیم بتواند در پایان دوره به بیمار تحویل دهد.
1) اصول کلی نگهدارنده
چرا نگهدارنده؟ rTMS «حساسیت به تغییر» شبکههای مغزی را بالا میبرد؛ با چند جلسهی فاصلهدار، این تغییرات تحکیم میشوند و ریسک عود پایین میآید.
قاعدهٔ فاصلهدهی: ابتدا تراکم بالا → کاهش تدریجی (taper). برای بیماران پرریسک، از بوسترهای خوشهای (cluster) استفاده کنید.
بوسترهای خوشهای (cluster)» یعنی بهجای یک جلسه نگهدارندهی تکوتوکِ پراکنده، چند جلسهی تقویتی فشرده را در یک بازهی کوتاه پشتسرهم میچینیم تا اثر دورهی اصلی rTMS تثبیت شود و جلوی عود زودهنگام گرفته شود.
پایش مبتنی بر داده: حداقل هفتگی در ماه اول و سپس دوهفتهیکبار: PHQ-9/BDI-II (افسردگی)، GAD-7 (اضطراب)، Y-BOCS (OCD)، PCL-5 (PTSD)، HIT-6 (میگرن)، و شاخصهای عملکردی (خواب/انرژی/تمرکز/کارکرد اجتماعی).
2) برنامههای نگهدارنده برحسب اختلال (Ready-to-Use)
2.1 افسردگی (MDD/TRD)
کویل شکل ۸ | پروتکل پایانیافته: 10Hz چپ یا iTBS چپ
طرح Taper کلاسیک (پیشنهادی):
هفته 1–2: ۲ جلسه/هفته
هفته 3–4: ۱ جلسه/هفته
ماه 2–3: ۱ جلسه/هر ۲ هفته
ماه 4–6: ۱ جلسه/ماه (یا «on-demand»)
طرح Cluster (پرخطر/TRD):
هر ماه: ۵ جلسه در یک هفته (Mon–Fri) × ۳ ماه؛ سپس ماهانه ۱–۲ جلسه
Trigger بوستر فوری: افزایش ≥ ۵ امتیاز PHQ-9 نسبت به «کمترین» امتیاز بهمدت ≥ ۲ هفته یا افت کارکرد محسوس → ۳–۵ جلسه بوستر در ۷–۱۰ روز.
2.2 اضطراب (GAD/اجتماعی/پانیک)
Primary: 1Hz راست DLPFC ± iTBS چپ
هفته 1–4: ۱ جلسه/هفته
ماه 2–3: ۱ جلسه/هر ۲ هفته
ماه 4–6: ۱ جلسه/ماه
بوستر موقعیتی: پیش از رویدادهای استرسزا (امتحان/سفر/شغلی) ۱–۲ جلسه در ۳–۵ روز قبل.
2.3 وسواس (OCD)
Figure-8 روی SMA دوطرفه یا Deep-coil H7 روی mPFC/ACC
هفته 1–4: ۲ جلسه/هفته
ماه 2–3: ۱ جلسه/هفته
ماه 4–6: ۱ جلسه/هر ۲–۴ هفته
همراهی الزامی: ERP/CBT پیوسته؛ بدون ERP، نگهدارنده اثر کمتری دارد.
Trigger بوستر: افزایش ≥ ۶ امتیاز Y-BOCS یا برگشت آیینها → ۵–۱۰ جلسه خوشهای طی ۲ هفته.
2.4 PTSD
1Hz راست DLPFC یا پروتکلهای mPFC (Deep)
هفته 1–4: ۱ جلسه/هفته
ماه 2–3: ۱ جلسه/هر ۲ هفته
ماه 4–6: ۱ جلسه/ماه
همراهی: Trauma-focused CBT/EMDR.
بوستر: بازگشت کابوس/برانگیختگی → ۳–۵ جلسه در ۱۰ روز.
2.5 درد مزمن / میگرن
M1 کنترالترالِ محل درد | 10–20Hz
نگهدارندهٔ میگرن: هر ماه ۳ جلسه (روزهای متوالی) × ۳ ماه، سپس PRN
درد نوروپاتیک: ۱–۲ جلسه/هفته × ۴ هفته، سپس ۱ جلسه/هر ۲–۴ هفته (بر اساس VAS/HIT-6)
Trigger بوستر: افزایش VAS ≥2/10 برای ≥۵ روز یا افزایش HIT-6 ≥5 امتیاز.
2.6 ADHD (بزرگسال/نوجوان)
iTBS چپ یا 1Hz راست
هفته 1–4: ۱ جلسه/هفته + تمرینات شناختی
ماه 2–3: ۱ جلسه/هر ۲ هفته
ماه 4–6: ۱ جلسه/ماه
Trigger بوستر: افت عملکرد تحصیلی/شغلی + افزایش امتیاز ASRS → ۳ جلسه در یک هفته.
2.7 ترک نیکوتین
Deep H4 (اگر موجود) یا iTBS چپ بههمراه برنامه ترک
هفته 1–4: ۲ جلسه/هفته
ماه 2–3: ۱ جلسه/هفته
ماه 4–6: PRN (دوران لغزش/اشتیاق بالا)
بوستر در ریسک بالا: عود اخیر یا مناسبتهای محرک → ۳–۵ جلسه در ۷ روز.
نکتهٔ عملی: اگر دورهٔ حاد با iTBS بوده، نگهدارندهٔ iTBS (۳ دقیقهای) برای پایبندی بیمار بهتر جواب میدهد. اگر 10Hz بوده، میتوانید برای نگهدارنده به iTBS سوئیچ کنید تا زمان کلینیک آزاد شود.
3) الگوریتم «Recall» (فراخوانِ عود)
پایش خودکار:
هفته 2، 4، 8، 12 پس از اتمام دوره: تماس/فرم آنلاین (PHQ-9/GAD-7/… + ۳ شاخص عملکردی).
۳–۶ ماه: هر ماه یکبار چکاینِ کوتاه.
قواعد اقدام:
بوستر کوتاه (Rescue):
PHQ-9 ↑ ≥5 امتیاز (یا BDI-II ↑ ≥6) برای ≥۲ هفته، یا GAD-7 ↑ ≥4 → ۳–۵ جلسه در ۷–۱۰ روز
Mini-Acute:
بازگشت به ≥50% علائم پایه یا افت شدید کارکرد → ۱۰–۱۵ جلسه طی ۳ هفته
بازنگری درمان:
عدم پاسخ به Rescue/mini-acute → Case-conference (دارو/رواندرمانی/مسیر جایگزین)
4) پیامهای آمادهٔ Recall (SMS/WhatsApp)
۴۸ ساعت پس از اتمام دوره:
«سلام … عزیز. دوره rTMS شما تمام شد از این هفته هر ۷ روز یکبار یک فرم کوتاه دریافت میکنید (خلق/خواب/انرژی). اگر هر تغییری حس کردید، همینجا پیام بدید. تیم دانا ⚕️»هفته ۲ / ۴ / ۸ / ۱۲:
«فرم پایش هفتگی شما آماده است (کمتر از ۱ دقیقه). لطفاً تکمیل کنید تا در صورت نیاز، بوستر کوتاه را سریع شروع کنیم. »Trigger بوستر (آستانه رد شد):
«نتایج فرم اخیر نشان میدهد چند علامت برگشته. پیشنهاد: ۳ جلسه بوستر در ۷–۱۰ روز آینده. برای زمانبندی با پذیرش تماس بگیرید: 07136476172.»