مقدمه
دوپامین و سیستم دوپامینرژیک، مانند بسیاری از سیستمهای تعدیلکننده عصبی مغز، بر رفتارهای مختلفی اثر می گذارد. اینها شامل رفتارهایی مانند پاداشهای یادگیری، همکاری اجتماعی، رفتار هدفدار و تصمیمگیری می باشند. علاوه بر این، تغییرات در مدارهای دوپامینرژیک در مدلهای حیوانی و انسانها نشانه رفتارهای اعتیادآور است. احتمالاً نتیجه تغییرات در نحوه ارتباط نورونهای دوپامینرژیکی با اهداف مورد نظر است. با این حال، اطلاعات زیادی در مورد ترکیب مولکولی و نقشهای عملکردی نورونهای دوپامینرژیک در رفتار طبیعی و اعتیاد وجود دارد. اما اطلاعات کمتری در مورد نحوه ارتباط فیزیکی نورونهای دوپامینرژیک با اهداف و چگونگی تغییر آن ارتباط با قرار گرفتن در معرض مواد مخدر شناخته شده است. تا همین اواخر، جمع آوری و تجزیه و تحلیل حجم زیادی از بافت مغز با میکروسکوپ الکترونی (EM)، استاندارد طلایی برای تعیین اتصالات عصبی، دشوار و پر زحمت بود.
ویژگی های فراساختاری سیناپس های دوپامین
بر خلاف اتصالات تحریکی یا مهاری یونوتروپیک، اطلاعات کمتری در مورد ویژگی های فراساختاری سیناپس های دوپامینرژیک وجود دارد. بنابراین، تجزیه و تحلیل مدارهای DA نیاز به برچسب گذاری خاصی دارد. چه با ایمونوهیستوشیمی یا با هدف گیری ژنتیکی. با این حال، سؤالات اساسی بدون پاسخ باقی میمانند. (1) آکسونهای DA چند بار سیناپسهایی میسازند که شبیه سیناپسهای شیمیایی کلاسیک به نظر میرسند؟ (2) سیناپسهای DA در کجا روی نورونهای هدف رخ میدهند؟ (3) واریکوزیته های آکسون DA شامل چه چیزهایی هستند؟ (4) آیا نشانه هایی از سایر فعل و انفعالات فیزیکی بین آکسون های DA و اهداف آنها وجود دارد؟
ما چندین جنبه جدید از زیست شناسی آکسون دوپامینرژیک را یافتیم.
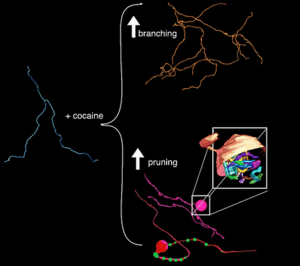
ما شواهد فراساختاری سیناپس ها، انواع مختلف واریکوزیته های آکسونی و شواهدی از “اسپینول ها” را بررسی کردیم. اسپینول ها جایی که غشاهای واریس آکسونی دوپامینرژیکی با غشای آکسون های تحریک کننده و بازدارنده مجاور در هم می آمیزند. همچنین دندریتهای نورونهای ساکن، که یادآور اسپینولها در سایر قسمتهای مغز هستند. قرار گرفتن کوتاه مدت در معرض کوکائین، شواهدی از بازآرایی آکسون ها در مقیاس بزرگ را نشان می دهد. 50 درصد از آکسون های دوپامینرژیک حاوی شاخه هایی هستند که به blind bulb ها ختم می شوند. که اغلب توسط زوائد پیچیده گلیاهای مجاور احاطه شده است.
خلاصه مطالعه و نقش دوپامین در اعتیاد
مطالعه تغییرات خاصی را نشان می دهد که در مغز موش هایی که در معرض کوکائین قرار دارند رخ می دهد. این یافته ها نقش دوپامین در اعتیاد را روشن می کند. بینش جدیدی در مورد انتقال دوپامین در مغز ارائه می دهد. محققان از فناوری پیشرفته و موشها برای مطالعه ساختار نورون دوپامین، اعتیاد و توانایی مغز برای بهبودی استفاده کردند. یک تبلیغ تجاری اواخر دهه 1980 برای مبارزه با اعتیاد به مواد مخدر از یک جفت تخم مرغ سرخ شده به عنوان استعاره ای از اثرات مواد مخدر بر مغز انسان استفاده کرد. در حالی که محققان مدتها متوجه شدهاند که بین مصرف مواد مخدر و تغییرات نامطلوب در مغز ارتباط وجود دارد. تنها اکنون میتوانند تغییراتی را که واقعاً رخ میدهند، با جزئیات دقیق مطالعه کنند.
محققان دانشگاه شیکاگو و آزمایشگاه ملی آرگون در وزارت انرژی ایالات متحده این مطالعه را انجام دادند.
با استفاده از فناوری پیشرفته، برای اولین بار تغییرات خاصی را که در مغز موش هایی که در معرض کوکائین قرار دارند رخ می دهد، تشریح کردند. این تحقیق بینش جدیدی را در مورد عملکرد ساختارهای عصبی دوپامین ارائه می دهد. نوروترانزمیتری که در عملکردهای متعدد، از حرکت داوطلبانه تا رفتار، دخیل است. محققان امیدوارند که بفهمند انواع خاصی از اعتیاد چگونه کار می کنند و احتمالاً درمان های هدفمندی را توسعه دهند.
این مقاله اخیراً در مجله eLife منتشر شده است.
محققان چگونگی ایجاد زمینههای رو به رشد کانکتومیک، توسعه نقشههای سه بعدی بسیار دقیق از هر نورون در مغز و اتصالات آنها را شرح میدهند. به نوبه خود، تیم تصمیم گرفت تا فرآیند انتقال دوپامین از طریق نورون ها را با وضوح بیشتری شناسایی کند. زیرا آنها اتصالات فیزیکی معمولی را ایجاد نمی کنند. جایی که سیگنال ها از طریق سیناپس ها منتقل می شوند. گرگ ویلدنبرگ، محقق ارشد این پروژه، است. «شواهد نشان میدهد که این نورونها دوپامین را به فضای خارج سلولی میریزند. درنتیجه نورونهای مجاور که گیرندههای حسگر دوپامین دارند را فعال میکنند. ”اما کانکتومیکس در مورد این نوع مدارها حرف چندانی برای گفتن نداشته است. زیرا آنها اتصالات معمولی ایجاد نمی کنند. بنابراین ما می خواستیم به این منطقه قدم بگذاریم تا ببینیم واقعاً چگونه کار می کند.”
انگیزه دیگر این پروژه، درک نقش دوپامین در اعتیاد بود.
در صورت وجود، چه تغییرات آناتومیکی در مدارهای دوپامین ناشی از مصرف مواد مخدر، مانند کوکائین است؟ به دست آوردن این سطح از جزئیات نیاز به استفاده از میکروسکوپ الکترونی سریال سه بعدی با حجم زیاد Argonne داشت. یک میکروسکوپ پرقدرت که قادر به تجسم کوچکترین جزئیات مغز بود. امکان دید صمیمانهتری به نورونهای دوپامین از مجموعهای از موشهای حساس به کوکائین و حیوانات کنترل را فراهم کرد. این تیم با استفاده از منابع دانشگاه شیکاگو، تقریباً 2000 بخش به ضخامت 40 نانومتر (1 میلیمتر = 1 میلیون نانومتر) را از بخشهای مرتبط با دوپامین در مغز میانی و جلوی مغز جمعآوری کردند. از این نمونهها، SEM مجموعهای از تصاویر دوبعدی و مجزا تولید کرد که در مجموع بیش از 1.5 ترابایت داده است. اینها به صورت دیجیتالی با استفاده از خوشه تجسم، کولی، در یک مرکز محاسبات دوباره مونتاژ شدند.
این فرآیند یک حجم سه بعدی ایجاد می کند.
پس به محققان اجازه می دهد ویژگی های آناتومیکی مختلف نورون های دوپامین را شناسایی و ردیابی کنند. که تا همین اواخر، یکی از چالش های مهم پیش روی محققان بود. ” ما در واقع میتوانیم تغییرات آناتومیکی را که ممکن است در هر نقطهای از مغز رخ دهد، تشخیص دهیم.” ”آیا میتوانیم این برش میکروسکوپی مغز را برداریم و چیزی را پیدا کنیم که از نظر کمی متفاوت باشد؟ این نیز بخشی از دلیلی است که ما کوکائین را انتخاب کردیم. زیرا فکر میکردیم هر اتفاقی که میافتد احتمالاً بهطور سیستماتیک در سراسر مغز اتفاق میافتد.» نتایج نشان داد که در واقع، نورونهای دوپامین به جز در موارد نادر، اتصالات فیزیکی برقرار نمیکنند. و دومی ممکن است نشان دهد که نورون های دوپامین یکسان نیستند. که ممکن است یک زیر کلاس متفاوت وجود داشته باشد که تمایل به ایجاد ارتباطات فیزیکی بیشتر دارد.
آنچه پژوهشگران دریافتند
به طور کلی، آنها دریافتند که تورمهای کوچک یا واریکوسیتهها – محلهایی که مسئول ترشح دوپامین هستند – میتوانند به چهار نوع مختلف طبقهبندی شوند. تا حدی بر اساس اندازه و همچنین مقدار وزیکولهای حامل انتقالدهنده عصبی که در هر واریس وجود دارد. آنها دریافتند که برخی از این تورمها فاقد هر گونه وزیکول هستند. که باعث شد برخی از منتقدان ادعا کنند که نمیتوان آنها را به عنوان مکانهای انتشار مناسب تعریف کرد. آنها می گویند که این واریس های خالی احتمالاً نشان می دهد که ممکن است اجزای مولکولی دیگری، علاوه بر حضور وزیکول، وجود داشته باشد که مکان های آزادسازی دوپامین را مشخص می کند.
“ما پیشنهاد میکنیم که این واریسهای خالی تمام ماشینهای مولکولی برای آزادسازی دوپامین را داشته باشند. اما ممکن است که وزیکولهای دوپامین به طور فعال در سراسر آکسون جابجا شوند و ما بهطور اتفاقی به موقع یک عکس فوری از جایی که برخی از آنها خالی هستند، بگیریم.»
بخش کوکائین این مطالعه دو تغییر عمده را به همراه داشت که هر دو بر آکسونها تمرکز دارند.
آکسون ها زائده های بسیار نازکی اند که از نورونها خارج میشوند. مانند درختان، از آکسون ها شاخه هایی جوانه می زنند که به سمت آکسون های دیگر منشعب می شوند تا سیگنال ها را ارسال کنند. پس از قرار دادن موش ها در معرض کوکائین، تیم متوجه افزایش آن شاخه شد. در یک نتیجه کاملاً غیرمنتظره، آنها همچنین دریافتند که حدود نیمی از آکسونهایی که مورد مطالعه قرار گرفتند، تورمهای بزرگ در مکانهای مختلف در امتداد آکسون تشکیل دادند. نزدیک ترین همبستگی با این تورم های در حال رشد، در محل اتصال نورون ها به ماهیچه ها ظاهر می شود. در برخی موارد، آکسون جمع میشود یا هرس میشود و سپس به یک ساختار پیاز مانند بزرگ متورم میشود. این تیم نشانه هایی از جوانه زدن و عقب نشینی را دیدند.
منبع: Study Highlights Connections Between Addictive Drugs and Brain Function in Mice – Neuroscience News