خلاصه مطالعه:
به نظر می رسد پروتئینی به نام Tmep با تغییر رفتار یک کانال یونی تحریک پذیری نورون را کنترل می کند. بر احتمال فعالیت آن نورون تأثیر می گذارد. این می تواند یکی از علل ناشتاخته صرع باشد.
صرع یک بیماری شایع است که بر مغز تأثیر می گذارد. باعث تشنج های مکرر می شود. تشنج انفجاری از فعالیت الکتریکی در مغز است که به طور موقت بر نحوه عملکرد آن تأثیر می گذارد. آنها می توانند طیف گسترده ای از علائم را ایجاد کنند. صرع می تواند در هر سنی شروع شود. اما معمولا در دوران کودکی یا در افراد بالای 60 سال شروع می شود.
صرع یک اختلال مغزی است که با تشنج های مکرر مشخص می شود. تشنج معمولاً به عنوان یک تغییر ناگهانی رفتار به دلیل تغییر موقت در عملکرد الکتریکی مغز تعریف می شود. به طور معمول، مغز به طور مداوم تکانه های الکتریکی کوچک را در یک الگوی منظم تولید می کند.
منبع: دانشگاه آریزونا
مقدمه
به گفته موسسه ملی اختلالات عصبی و سکته، در بسیاری از موارد صرع – اختلالی که الگوی طبیعی فعالیت الکتریکی مغز را مختل می کند و اغلب منجر به تشنج می شود – علت اصلی ناشناخته است.
محققان دانشگاه آریزونا ممکن است توضیحی برای برخی از اشکال صرع پیدا کرده باشند. نتایج آنها در Molecular Neurobiology منتشر شده است. محققان ژنی را در موشها مطالعه کردند. این ژن بر شکلگیری و عملکرد اتصالات بین عضله و نورونهای حرکتی که حرکت بدن را کنترل میکنند، تأثیر میگذارد.
تیفانی چو، سرپرست تیم تحقیق، که تکنسین تحقیقاتی در آزمایشگاه UArizona Bhattacharya بود. گفت: آنها کشف کردند که وقتی پروتئینی به نام TMEM184B، که در غشای سلولی نورون ها وجود دارد، وجود ندارد، نورون ها آسیب دیده و اغلب فعال می شوند. چو در پاییز به عنوان دانشجوی پزشکی در دانشکده پزشکی دانشگاه لیبرتی در ویرجینیا شروع به کار خواهد کرد.
محققان تعجب کردند که چگونه نورونهای به ظاهر آسیبدیده ممکن است بر توانایی فعالیت نورون بر عملکرد صحیح عضلات تأثیر بگذارند.
بنابراین، چو و همکارانش بعداً پروتئین مربوطه به نام Tmep را در مگسهای میوه بررسی کردند. پروتئینی که مطالعه آن در سطح سلولی آسانتر است. مارتا باتاچاریا، استادیار دپارتمان علوم اعصاب و مدیر آزمایشگاه باتاچاریا، که مراحل اولیه زوال بیماری را بررسی میکند. وی گفت: «آنچه در مگسهای میوه یافتیم این بود که به نظر میرسد نورونها به یک محرک فردی بیش از حد واکنش نشان نمیدهند. این مورد سلامت سلول های مغز در بیماری های عصبی را تحت تاثیر قرار می دهد.
این نشان می دهد که:
Tmep – و TMEM184B به طور گسترده – مسئول کنترل تحریک پذیری نورون ها هستند. بهتاچاریا گفت: “این به اتفاقی که برای بیماران مبتلا به صرع می افتد مربوط می شو. بنابراین ما فکر می کنیم که ممکن است ژنی را شناسایی کرده باشیم که در برخی از اشکال صرع دخیل است. یعنی زمانی که توضیح دیگری برای علت صرع وجود ندارد.”
محققان فکر میکنند که Tmep ممکن است رفتار کانالهای یونی را که میزان کلسیم در سلول را کنترل میکنند. در نتیجه احتمال شلیک نورون را تغییر دهد. وقتی تغییرات سلولی را در مگسهای میوه دیدیم، واقعاً باعث شد به این فکر کنیم که آیا این هم تعادل یونها را کنترل میکند. مثلاً ذرات باردار مانند کلسیم در نورونها، زیرا این یک اتفاق رایج در صرع است. تا این مقاله هیچ کس به این موضوع توجه نکرده بود که آیا این پروتئین سطح یون را کنترل می کند یا خیر.
ما میتوانیم این کار را در مدل مگس میوه انجام دهیم زیرا:
روشهایی برای اندازهگیری فعالیت الکتریکی داریم و این کاری است که در مقاله انجام دادیم. کاری که ما میخواهیم انجام دهیم این است که آن جهشهای انسانی را در ژنوم مگس قرار دهیم. ببینیم که آیا آنها همان تغییرات را در تحریک پذیری نورونها ایجاد میکنند یا خیر. بنابراین می توانیم مکانیسم های مربوط به صرع را بیشتر بدانیم.
اگر آنها این کار را انجام دهند، ما میخواهیم دلیل آن را بدانیم.» محققان همچنین متوجه شدند که لارو مگس بدون Tmep هنگام خزیدن روی صفحه بسیار کندتر از سایر مگس ها حرکت می کند.
در نتیجه، آنها کنجکاو هستند که ببینند آیا این پروتئین علاوه بر اختلالاتی مانند صرع، ممکن است در سایر بیماریهای عصبی عضلانی مانند اسکلروز جانبی آمیوتروفیک یا ALS نیز نقش داشته باشد.
خلاصه
مگس سرکه TMEM184B Ortholog Tmep با مهار شلیک نابجا در محل اتصال عصبی عضلانی، حرکت مناسب را تضمین می کند. TMEM184B یک پروتئین غشایی هفت بار گذرنده از غشاء است. باعث دژنراسیون آکسون پس از آسیب می شود. جهش TMEM184B باعث ایجاد ساختار عصبی عضلانی ناهنجار می شود. نقص های رفتاری حسی و حرکتی در موش ایجاد می کند. مکانیسمی که از طریق آن TMEM184B باعث ایجاد نقص عصبی عضلانی می شود ناشناخته است.
ما از مگس سرکه ملانوگاستر برای بررسی عملکرد ژن مرتبط نزدیک، Tmep (CG12004)، در محل اتصال عصبی عضلانی استفاده کردیم. ما نشان میدهیم که Tmep برای زنده ماندن کامل بزرگسالان و حرکت کارآمد لارو مورد نیاز است.
لاروهای جهش یافته Tmep دارای نرخ انقباض بدنی کمتری نسبت به گروه شاهد هستند. در مادهها کمبودهای قویتری دیده می شود. در عضلات دیواره بدن، جهشیافتههای Tmep بیشتحریکپذیری قابلتوجهی را نشان میدهند. همچنین بسیاری از پتانسیلهای پس سیناپسی که در پاسخ به یک تحریک منفرد فعال میشوند. این موارد مطابق با نقش Tmep در مهار تحریکپذیری سیناپسی است.
در اتصالات عصبی عضلانی جهش یافته Tmep:
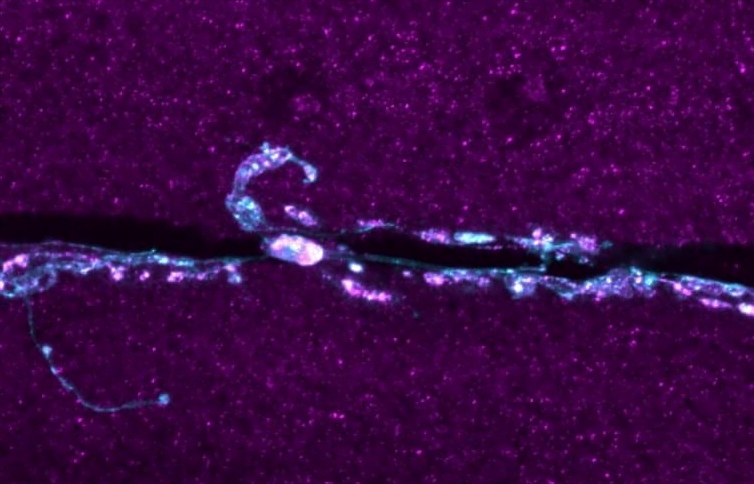
سازگاری با رشد بیش از حد سیناپسی وابسته به فعالیت دیده می شود. Tmep در اندوزومها و وزیکولهای سیناپسی درون نورونهای حرکتی بیان میشود. نقش احتمالی در جا به جایی غشای سیناپسی را نشان میدهد. با استفاده از RNAi knockdown، نشان میدهیم که Tmep در نورونهای حرکتی برای حرکت و تحریکپذیری مناسب لارو مورد نیاز است. کاهش آن باعث افزایش سطح کلسیم پیشسیناپسی میشود.
نقایص حرکتی را می توان با ناک داون پیش سیناپسی کانال های کلسیم شبکه آندوپلاسمی یا با کاهش احتمال رهاسازی برانگیخته نجات داد. اینها بیشتر نشان می دهد که فعالیت سیناپسی بیش از حد منجر به کمبودهای رفتاری می شود. کار ما یک عملکرد حیاتی برای Tmep در تنظیم انتقال سیناپسی و رفتار حرکتی ایجاد می کند.
چنتن چه از اختلالاتی مانند صرع رنج می برید، ما در انستیتو سلامت مغز دانا در کنارتان هستیم.
منبع: New Research Could Explain Unknown Causes of Epilepsy – Neuroscience News