دانشمندان دانشکده پزشکی Icahn School of Medicine نقش جدیدی را برای دوپامین شیمیایی مغز کشف کرده اند که مستقل از عملکرد آن به عنوان ارتباطات عصبی است. براساس مطالعه ای منتشر شده در روز جمعه، 10 آوریل در ژورنال Science، نقش جدید به نظر می رسد به عنوان تغییر در بیان ژن مرتبط با قرار گرفتن در معرض مزمن یا سوء مصرف کوکائین است.
ایان ماز، دانشیار علوم اعصاب و علوم فارماکولوژیکی، در دانشکده پزشکی ایکان اظهار می کند: “مطالعه ما اولین شواهد را ارائه می دهد که چگونه دوپامین می تواند به طور مستقیم بر ناهنجاری های بیان ژن ناشی از سوء مصرف دارو و رفتار پس از آن تأثیر بگذارد.”
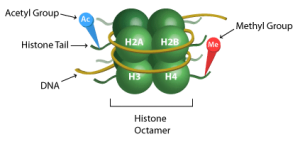
وی ادامه داد: به غیر از انتقال سیگنال ها بین سلولهای عصبی در مغز، ما دریافتیم كه دوپامین می تواند از نظر شیمیایی به پروتئین های هیستون متصل شود، این امر باعث می شود سلول ها ژن های مختلف را روشن و خاموش كنند و مناطقی از مغز را كه درگیر انگیزه و رفتار پاداش هستند، تحت تأثیر قرار می دهد. فرآیند بیوشیمیایی به میزان قابل توجهی منجر به آسیب پذیری و عود کوکائین در اثر سوء مصرف مواد مخدر می شود. “
این تحقیق حول محور DNA و نحوه کار در شکل گیری نقشه بیولوژیکی فردی هر شخص می چرخد. هر سلول بدن حاوی نوکلئوزوم است، این DNA در اطراف پروتئین های هیستون پیچیده (پروتئین هایی که DNA را در هسته سلول ها بسته بندی می کنند، و به شدت مستعد تغییرات شیمیایی هستند که به تنظیم بیان ژن کمک می کنند) و ساختارهایی را به نام نوکلئوزوم به وجود می آورد.
هنگامی که DNA کد کننده یک ژن خاص در محفظه ای محکم پیچیده می شود، احتمالاً این ژن کمتر بیان می شود. این می تواند بسیاری از کارکردهای سلول را تحت تأثیر قرار دهد.
دوپامین، به عنوان انتقال دهنده عصبی “احساس خوب” شناخته می شود، یک ماده شیمیایی که اطلاعات بین سلول های عصبی را تأمین می کند. مغز هنگام وقایع خوشایند، آن را آزاد می کند و به عنوان بخشی از سیستم پاداش طبیعی برای احساس لذت و رضایت است.
این ماده عصبی شیمیایی مهم برای انگیزه و توجه را تقویت می کند و به تنظیم حرکت، یادگیری و واکنش های عاطفی کمک می کند. دوپامین همچنین ما را قادر می سازد که نه تنها جوایزی را ببینیم بلکه برای حرکت به سمت آنها نیز اقدامی انجام دهیم.
اعتقاد بر این است که آسیب پذیری برای عود سوء مصرف مواد، در دوره های ترک کوکائین ناشی از فراخوانی وبازخوانی مدار پاداش مغز، به ویژه در مناطق میانی مغز، مانند منطقه (VTA) است.
این تیم تحقیقاتی دریافتند که پروتئینی به نام ترانس گلوتامیناز 2 می تواند مستقیماً مولکول های دوپامین را به پروتئین های هیستون متصل کند (فرآیندی به نام دوپامینیلاسیون هیستون یا H3Q5dop) که به نوبه خود بر روی هیستون-DNA اثر می گذارد تا بتواند تغییرات محیطی را در بیان ژن تنظیم کند.
آنها دریافتند که دوپامینیلاسیون هیستون نقش مهمی در تقویت آسیب پذیری افزایش یافته به عود در مدت زمان طولانی دارد. به طور خاص، تجمع H3Q5dop در VTA، در حقیقت، می تواند مدار پاداش را ربوده و تمایز بین رفتار خوب و ناسازگار را دشوار کند.
با این حال، این مطالعه نشان داد كه كاهش H3Q5dop در موشهای صحرایی كه برای ترک كوكائین برنامه ریزی شده بودند، به طور قابل ملاحظه ای تغییرات بیان ژن با كوكائین را معكوس كرده و باعث كاهش رفتار مربوط به سوء مصرف كوكائین می شود.
اشلی لپاک، محقق گروه علوم اعصاب موسسه مغز فریدمن: “سوالی که همواره دانشمندان علوم اعصاب را به چالش کشیده این است که، چه پدیده های اساسی مولکولی باعث افزایش آسیب پذیری در برابر عود مواد مخدر در افراد می شود.”
تحقیقات ما با شناسایی دوپامینیلاسیون هیستون به عنوان یک نقش مستقل از انتقال دهنده عصبی، برای دوپامین که قبلاً در آسیب شناسی مغز دخیل نبود، در این ناحیه درگیری چشمگیر خود را به نمایش می گذارد. “
“ما معتقدیم که این یافته ها نشانگر تغییر پارادایم در نحوه تفکر درباره نقش دوپامین است، نه تنها در زمینه سوء مصرف مواد مخدر، بلکه به طور بالقوه در سایر رفتارها و اختلالات مرتبط با پاداش و همچنین در بیماریهای عصبی مانند پارکینسون، که در آن سلولهای عصبی دوپامین نقش دارد. “
در مطالعهای که سال گذشته منتشر شد، دکتر ماز و تیمش دریافتند که انتقال دهنده عصبی دیگری به نام سروتونین، یک ماده شیمیایی که در تنظیم خلقی دخیل است، به روشی مشابه دوپامین روی بیان ژن در سلولهای مغزی عمل می کند.
هنگامی که ما این مکانیسم سیگنالینگ منحصر به فرد را با سروتونین مشاهده کردیم، تصمیم گرفتیم به انتقال دهنده های عصبی دیگر، به ویژه دوپامین، توجه کنیم و دریافتیم که می تواند این عمل را انجام دهد.”
برای اطلاعات بیشتر به موسسه سلامت مغز دانا مراجعه کنید.
منبع: